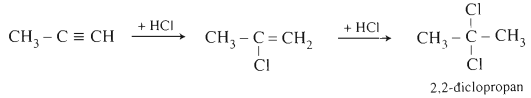Hoá học 11 Bài 32: Ankin
Tóm tắt bài
1.1. Đồng đẳng, đồng phân, danh pháp
Ankin: là những hidrocacbon mạch hở có 1 liên kết 3 (C≡C) trong phân tử.
1.1.1. Dãy đồng đẳng của ankin
- Dãy đồng đẳng của ankin: C2H2, C3H4, … CnH2n-2 (n ≥2)
- Công thức electron:
- Công thức cấu tạo: \(H - C \equiv C - H\)
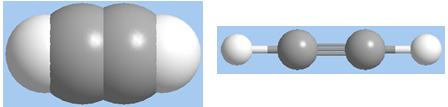
Hình 1: Mô hình phân tử axetilen dạng đặc và dạng rỗng
1.1.2. Đồng phân
- Hai chất đầu dãy C2, C3 không có đồng phân ankin.
- Các ankin từ C4 trở lên có đồng phân vị trí liên kết ba
- Từ C5 còn có đồng phân mạch Cacbon (tương tự anken)
Ví dụ: Đồng phân C4H6
CH≡C−CH2−CH3: but-1-in (Etyl axetilen)
CH3−C≡C−CH3: but-2-in (Đimetyl axetilen)
Ví dụ: Đồng phân C5H8
CH≡C−CH2−CH2−CH3: pent-1-in (Propyl axetilen)
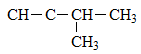
CH3−C≡C−CH2−CH3: pent-2-in (Etyl metyl axetilen)
1.1.3. Danh pháp
a) Tên thông thường
b) Tên thay thế:
Số chỉ vị trí-tên nhánh|tên mạch chính|-số chỉ vị trí-in
Các ankin có liên kết ba đầu mạch (dạng \(R - C \equiv CH\))
1.2. Tính chất vật lí
- Ankin có nhiệt độ sôi tăng dần theo chiều tăng của phân tử khối.
- Ankin có nhiệt độ sôi cao hơn và khối lượng riêng lớn hơn các anken tương ứng.
- Các ankin không tan trong nước và nhẹ hơn nước.
1.3. Tính chất hóa học
- Nguyên tử C của liên kết 3 ở trạng thái lai hoá sp (lai hoá phẳng) → (HCC) = 1800.
- Liên kết 3 C≡C gồm 1 liên kết \(\sigma\) và 2 liên kết \(\pi\)
1.3.1. Phản ứng cộng
a. Cộng Hidro
Dùng Pb/PdCO3 hoặc Pd/BaSO4. Ankin chỉ cộng một phân tử hidro tạo anken.
CH≡CH + H2 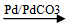
CH≡CH + 2H2 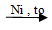
b. Cộng Br2:
c. Cộng HCl
CH≡CH + HCl 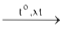
CHCl═CH2 +HCl 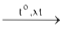
d. Cộng nước (hiđrat hoá)
CH≡CH + H2O 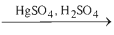
Lưu ý: Phản ứng cộng HX, H2O vào các ankin trong dãy đồng đẳng của axetilen cũng tuân theo quy tắc Maccopnhicop như anken.
e. Phản ứng đimehoá, trimehoá.
2 CH≡CH .PNG)
3 CH≡CH .PNG)
1.3.2. Phản ứng thế bằng ion kim loại
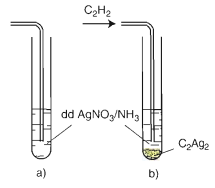
Hình 2: Phản ứng thế nguyên tử Hidro của C2H2 bằng ion bạc
a) trước khi sục khí C2H2
b) Sau khi sục khí C2H2
CH≡CH + 2AgNO3 + 2 NH3 → AgC≡CAg ↓vàng + 2 NH4NO3
- Nguyên tử H đính với C mang liên kết 3 linh động hơn rất nhiều so với C liên kết đôi, đơn => nó có thế bởi ion KL.
- Phản ứng này dùng để nhận biết các ankin 1 (có liên kết 3 ở đầu mạch)
RC≡CH + 2 AgNO3 + 2 NH3→ RC≡CAg + 2 NH4NO3
1.3.3. Phản ứng oxi hoá
a. Phản ứng oxi hoá hoàn toàn
2CnH2n-2 + (3n -1)O2 → 2n CO2 + 2(n-1) H2O
b. Phản ứng oxi hoá không hoàn toàn
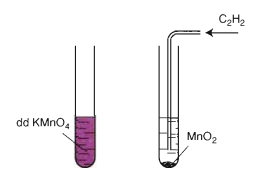
Mất màu KMnO4
Hình 3: Axetilen làm mất màu dd thuốc tím
1.4. Điều chế
1.4.1. Phòng thí nghiệm
CaC2 + H2O → Ca(OH)2 + C2H2 ↑
1.4.2. Công nghiệp
- Đi từ dầu mỏ:
2 CH4 → C2H2 + 3 H2 (ĐK: 1500oC)
- Đi từ đá vôi:
CaCO3 → CaO → CaC2 → C2H2
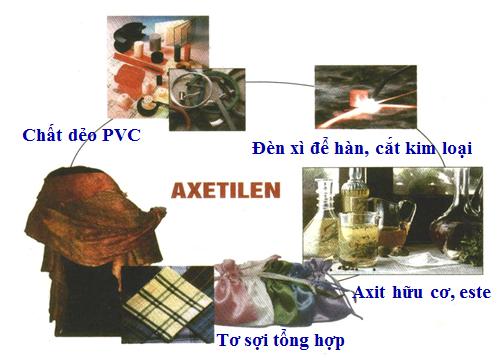
1.5. Ứng dụng
- Dùng trong CN hàn cắt KL
- Nguyên liệu tổng hợp chất hữu cơ cơ bản.
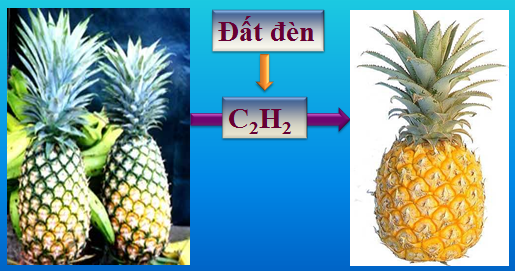
Hình 4: ứng dụng của axetilen
Hình 5: Đất đèn làm trái cây mau chín
Bài 1:
Khi điều chế axetilen bằng phương pháp nhiệt phân nhanh CH4 thu được hỗn hợp A gồm axetilen, hydro và một phần metan chưa phản ứng. Tỷ khối hơi cuả A so với hydro bằng 5. Hiệu suất chuyển hóa metan thành axetilen là:
Hướng dẫn:
Xét 1 mol CH4
2CH4 → C2H2 + 3H2
x → 0,5x → 1,5x mol
⇒ Sau phản ứng: nhh = 1 + x (mol)
Bảo toàn khối lượng: mtrước = msau
⇒ 16.1 = 5.2.(1 + x)
⇒ x = 0,6 mol
⇒ H% = 60%
Bài 2:
Một hidrocacbon X mạch thẳng có CTPT C6H6. Khi cho X tác dụng với dung dịch AgNO3/NH3 dư thu được hợp chất hữu cơ Y có MY - MX = 214 đvc. Xác định CTCT của X?
Hướng dẫn:
Vì X phản ứng với AgNO3/NH3 ⇒ X có nhóm -C ≡ CH đầu mạch
Công thức tổng quát: CxHy(C ≡ CH)n
CxHy(C ≡ CH)n → CxHy(C ≡ CAg)n
⇒ MY – MX = 107x = 214 ⇒ n = 2
Vì X mạch thẳng ⇒ X là CH ≡ C – CH2 – CH2 – C ≡ CH
Bài 3:
Nung nóng bình kín chứa 0,5 mol H2 và 0,3 mol ankin X (có bột Ni xúc tác), sau một thời gian thu được hỗn hợp Y. Tỉ khối của Y so với H2 bằng 16,25. Hỗn hợp Y phản ứng tối đa với 32 gam Br2 trong dung dịch. Công thức phân tử của X là:
Hướng dẫn:
\(n_{Br_{2}} = n_{pi(Y)}= 0,2 mol; \ n_{pi}\) (hh đầu) \(= 2n_{ankin} = 0,6 \ mol\)
⇒ \(n_{H_{2}}\) pứ \(=n_{pi}\) (hh đầu) \(- \ n_{pi(Y)} = 0,4 \ mol\)
⇒ sau phản ứng \(n_{Y} = n_{X} – n\) \(- n_{H_{2}}\) pứ \(= 0,5 + 0,3 - 0,4 = 0,4 \ mol\)
\(m_{X} = m_{Y} = M_{Y} \times n_{Y} = 16,25 \times 2 \times 0,4 = 13 \ g\)
⇒ \(m_{X}= 13 = 0,5 \times 2 + 0,3 \times M_{X}\)
⇒ \(M_{X} = 40 (C_{3}H_{4})\)
3. Luyện tập Bài 32 Hóa học 11
Sau bài học cần nắm:
- Khái niệm đồng đẳng, đồng phân, danh pháp & CTPT của ankin
- Phương pháp điều chế, ứng dụng của axetilen. Sự giống và khác về tính chất hoá học giữa ankin và anken.
3.1. Trắc nghiệm
Bài kiểm tra Trắc nghiệm Hóa học 11 Bài 32 có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
-
- A. CnH2n (n ≥ 2).
- B. CnH2n-6 (n ≥ 6).
- C. CnH2n+2 (n ≥ 1).
- D. CnH2n-2 (n ≥ 2).
-
- A. 4.
- B. 5.
- C. 2.
- D. 3.
-
Câu 3:
Cho propin tác dụng với dung dịch KMnO4 sau khi phản ứng xảy ra hoàn toàn, sản phẩm thu được gồm?
- A. CH3COOH, CO2, KOH, MnO2 và H2O.
- B. CH3COOK, K2CO3, KHCO3, MnO2 và H2O.
- C. CH3COOK, KHCO3, MnO2 và H2O.
- D. CH3COOK, K2CO3, MnO2 và H2O.
-
- A. 9,875.
- B. 10,53.
- C. 11,29.
- D. 19,75.
Câu 3- Câu 5: Xem thêm phần trắc nghiệm để làm thử Online
3.2. Bài tập SGK và Nâng cao
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 11 Bài 32.
Bài tập 32.3 trang 49 SBT Hóa học 11
Bài tập 32.4 trang 49 SBT Hóa học 11
Bài tập 32.5 trang 50 SBT Hóa học 11
Bài tập 32.6 trang 50 SBT Hóa học 11
Bài tập 32.7 trang 50 SBT Hóa học 11
Bài tập 32.8 trang 50 SBT Hóa học 11
Bài tập 1 trang 178 SGK Hóa học 11 nâng cao
Bài tập 2 trang 178 SGK Hóa học 11 nâng cao
Bài tập 3 trang 179 SGK Hóa học 11 nâng cao
Bài tập 4 trang 179 SGK Hóa học 11 nâng cao
Bài tập 5 trang 179 SGK Hóa học 11 nâng cao
Bài tập 6 trang 179 SGK Hóa học 11 nâng cao
4. Hỏi đáp về Bài 32 Chương 6 Hóa học 11
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa HOC247 thảo luận và trả lời nhé.
Bạn có biết?
Hóa học, một nhánh của khoa học tự nhiên, là ngành nghiên cứu về thành phần, cấu trúc, tính chất, và sự thay đổi của vật chất.Hóa học nói về các nguyên tố, hợp chất, nguyên tử, phân tử, và các phản ứng hóa học xảy ra giữa những thành phần đó.Hóa học đôi khi được gọi là "khoa học trung tâm" vì nó là cầu nối các ngành khoa học tự nhiên khác như vật lý học, địa chất học và sinh học.
Nguồn : Wikipedia - Bách khoa toàn thưTâm sự Lớp 11
Lớp 11 - Năm thứ hai ở cấp trung học phổ thông, gần đến năm cuối cấp nên học tập là nhiệm vụ quan trọng nhất. Nghe nhiều đến định hướng sau này rồi học đại học. Ôi nhiều lúc thật là sợ, hoang mang nhưng các em hãy tự tin và tìm dần điều mà mình muốn là trong tương lai nhé!
Nguồn : ADMIN :))Copyright © 2021 HOCTAPSGK

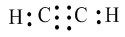
.PNG)