Hoá học 9 Bài 46 Mối liên hệ giữa etilen, rượu etylic và axit axetic
Tóm tắt bài
1.1. Mối liên hệ giữa etilen, rượu etylic và axit axetic
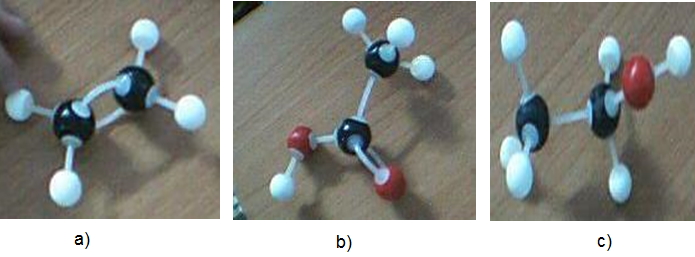
a) Cấu trúc của Etilen, Rượu etylic và Axit axetic
Hình 1: Cấu trúc của Etilen, Rượu etylic và Axit axetic
a) Etilen b) Rượu etylic c) Axit axetic
b) Sơ đồ mối liên hệ giữa các chất
Hình 2: Sơ đồ minh họa mối liên hệ giữa Etilen, Rượu etylic và Axit axetic
Ví dụ: Hoàn thành chuỗi phản ứng sau: C2H4 \(\overset{(1)}{\rightarrow}\) C2H5OH \(\overset{(2)}{\rightarrow}\) CH3COOH \(\overset{(3)}{\rightarrow}\) CH3COOC2H5
Phương trình phản ứng:
(1) C2H4(k) + H2O(l) \(\overset{Axit}{\rightarrow}\) C2H5OH
(2) C2H5OH + O2 \(\overset{men giam}{\rightarrow}\) CH3COOH+ H2O
(3) C2H5OH + CH3COOH .PNG)
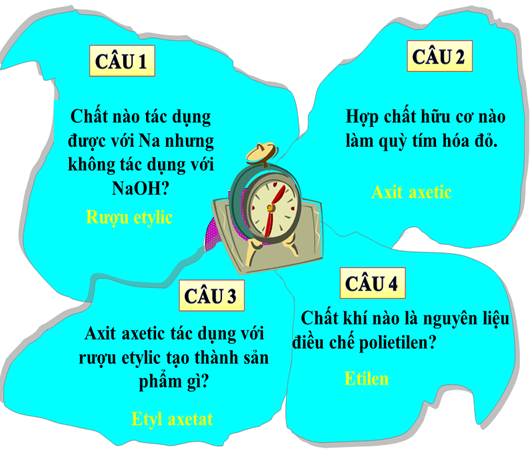
1.2. Tổng kết
Hình 3: Câu hỏi tổng kết về Etilen, Rượu Etylic, Axit axetic và Etyl Axetat
Bài 1:
Nêu hai phương pháp hóa học khác nhau để phân biệt hai dung dịch C2H5OH và CH3COOH
Hướng dẫn:
Có hai phương pháp dùng nhận biết hai dung dịch C2H5OH và CH3COOH như sau:
Phương pháp 1:
- Thuốc thử: Qùy tím
- Hiện tượng:
- Dung dịch CH3COOH: quỳ tím hóa đỏ.
- Dung dịch C2H5OH không làm đổi màu quỳ tím
Phương pháp 2:
- Thuốc thử: Dùng muối của axit yếu như Na2CO3 hoặc CaCO3
- Hiện tượng:
- Dung dịch CH3COOH có khí CO2 thoát ra do phản ứng: 2CH3COOH + CaCO3 → (CH3COO)2Ca + CO2\(\uparrow\) + H2O
- Dung dịch C2H5OH không có phản ứng.
Bài 2:
Cho 22,4 lít khí etilen (ở điều kiện tiêu chuẩn) tác dụng với nước có axit sunfuric làm xúc tác, thu được 13,8 gam rượu etylic. Hãy tính hiệu suất phản ứng cộng nước của etilen.
Hướng dẫn:
Số mol khí etilen là: \({n_{{C_2}{H_4}}} = \frac{{22,4}}{{22,4}} = 1(mol)\)
Phương trình phản ứng :
C2H4(k) + H2O(l) \(\overset{Axit}{\rightarrow}\) C2H5OH
1(mol) → 1 (mol)
Khối lượng rượu etylic thu được theo lí thuyết là: 1. 46 = 46 (gam)
Ta có khối lượng rượu etylic thu được thực tế là 13,8 gam
Hiệu suất của phản ứng công nước của etilen là: \(H = \frac{{{m_{tt}}}}{{{m_{lt}}}}.100 = \frac{{13,8}}{{46}}.100 = 30\%\)
Bài 3:
Tính khối lượng dung dịch axit axetic thu được khi lên men 5 lít rượu 400. Biết khối lượng riêng của rượu etylic là 0,8 g/ml và hiệu suất của quá trình lên men là 92%.
Hướng dẫn:
Ta có trong 5 lít rượu 400 có \(\frac{{5.40}}{{100}} = 2\) lít rượu nguyên chất. Vậy khối lượng rượu etylic có trong 5 lít rượu 400 là:
m = D.V = 0,8.2.1000 = 1600 (gam)
Vì hiệu suất của phản ứng đạt 92% nên khối lượng của rượu etylic đem lên men là: 1600. 0,92 = 1472
Số mol rượu etylic đem lên men là: \(\frac{{1472}}{{46}} = 32(mol)\)
Phương trình phản ứng:
C2H5OH + O2 \(\overset{men giam}{\rightarrow}\) CH3COOH+ H2O
32 (mol) → 32 (mol)
Khối lượng axit axetic thu được là: 32.60 = 1920 (gam)
3. Luyện tập Bài 46 Hóa học 9
Sau bài học cần nắm: Mối liên hệ giữa etilen, rượu etylic và axit axetic
3.1. Trắc nghiệm
Bài kiểm tra Trắc nghiệm Hóa học 9 Bài 46 có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
-
- A. Na2CO3.
- B. NaOH.
- C. NaCl.
- D. Na.
-
- A. Etylen.
- B. Axit axetic
- C. Natri axetat
- D. Etyl axetat
-
- A. CH4.
- B. C6H6.
- C. C2H2.
- D. CH3CH2OH.
Câu 3- Câu 5: Xem thêm phần trắc nghiệm để làm thử Online
3.2. Bài tập SGK và Nâng cao
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 9 Bài 46.
Bài tập 1 trang 144 SGK Hóa học 9
Bài tập 2 trang 144 SGK Hóa học 9
Bài tập 3 trang 144 SGK Hóa học 9
Bài tập 4 trang 144 SGK Hóa học 9
Bài tập 5 trang 144 SGK Hóa học 9
Bài tập 46.1 trang 56 SBT Hóa học 9
Bài tập 46.2 trang 56 SBT Hóa học 9
Bài tập 46.3 trang 56 SBT Hóa học 9
Bài tập 46.4 trang 56 SBT Hóa học 9
Bài tập 46.5 trang 56 SBT Hóa học 9
4. Hỏi đáp về Bài 46 chương 5 Hóa học 9
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa HOC247 thảo luận và trả lời nhé.
Bạn có biết?
Hóa học, một nhánh của khoa học tự nhiên, là ngành nghiên cứu về thành phần, cấu trúc, tính chất, và sự thay đổi của vật chất.Hóa học nói về các nguyên tố, hợp chất, nguyên tử, phân tử, và các phản ứng hóa học xảy ra giữa những thành phần đó.Hóa học đôi khi được gọi là "khoa học trung tâm" vì nó là cầu nối các ngành khoa học tự nhiên khác như vật lý học, địa chất học và sinh học.
Nguồn : Wikipedia - Bách khoa toàn thưTâm sự Lớp 9
Lớp 9 - Là năm cuối ở cấp trung học cơ sở, sắp phải bước vào một kì thi căng thẳng và sắp chia tay bạn bè, thầy cô và cả kì vọng của phụ huynh ngày càng lớn mang tên "Lên cấp 3". Thật là áp lực nhưng các em hãy cứ tự tin vào bản thân là sẻ vượt qua nhé!
Nguồn : ADMIN :))Copyright © 2021 HOCTAPSGK