Hoá học 12 Bài 28: Luyện tập Tính chất của kim loại kiềm, kim loại kiềm thổ và hợp chất của chúng
Tóm tắt bài
2.1. Vị trí của kim loại kiềm, kiềm thổ trong Bảng hệ thống tuần hoàn và cấu hình electron
| Vị trí trong Bảng tuần hoàn | Cấu hình electron lớp ngoài cùng | Tính chất hóa học đặc trưng | Điều chế | |
| Kim loại kiềm | Nhóm IA | ns1 |
Có tính khử mạnh nhất trong các kim loại \(M\rightarrow M^{+} + e\) |
Điện phân muối halogen nóng chảy \(2MX\overset{dpnc}{\rightarrow}2M+X_{2}\) |
| Kim loại kiềm thổ | Nhóm IIA | ns2 |
Có tính khử mạnh chỉ sau kim loại kiềm \(M\rightarrow M^{2+}+2e\) |
\(MX_{2}\overset{dpnc}{\rightarrow}M+X_{2}\) |
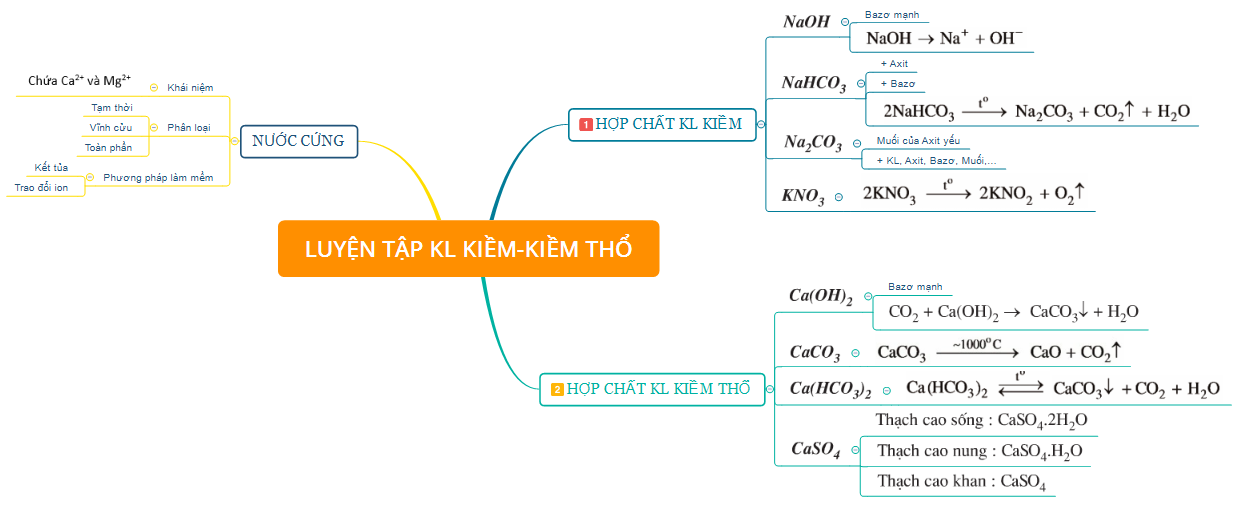
2.2. Một số hợp chất quan trọng của kim loại kiềm, kiềm thổ và Nước cứng
3.1. Bài tập Tính chất của kim loại kiềm, kim loại kiềm thổ và hợp chất của chúng - Cơ bản
Bài 1:
Hỗn hợp rắn A gồm Ca(HCO3); CaCO3; NaHCO3; Na2CO3. Nung A đến khối lượng không đổi được chất rắn B gồm:
Hướng dẫn:
Các muối hidrocacbonat của kim loại kiềm và kiềm thổ đều bị phân hủy tạo muối cacbonat khi ở nhiệt độ không quá cao, tuy nhiên chỉ có muối cacbonat của kim loại kiềm thổ mới bị thủy phân ở nhiệt độ cao tạo oxit kim loại.
⇒ Nhiệt phân hỗn hợp ban đầu sẽ thu được: CaO; Na2CO3.
Bài 2:
Cho các chất: Na2CO3; NaHCO3; NaHSO4; HCl; BaCl2; CuO; Fe. Số cặp chất có thể tác dụng trực tiếp với nhau ở nhiệt độ thường là:
Hướng dẫn:
Các cặp chất: (Na2CO3 + NaHSO4); (Na2CO3 + HCl); (Na2CO3 + BaCl2); (NaHCO3 + NaHSO4); (NaHCO3 + HCl); (NaHSO4 + BaCl2); (NaHSO4 + CuO); (NaHSO4 + Fe); (HCl + CuO); (HCl + Fe).
Bài 3:
Hoà tan hoàn toàn 14,52 gam hỗn hợp X gồm NaHCO3, KHCO3 và MgCO3 bằng dd HCl dư, thu được 3,36 lít khí CO2 (đktc) và dd chứa m gam muối KCl. Giá trị của m là:
Hướng dẫn:
Coi hỗn hợp gồm KHCO3 và MgCO3 có số mol lần lượt là x và y (vì \(M_{NaHCO_{3}}= M_{MgCO_{3}}\))
\(\\ n_{CO_{2}}= 0,15 \ mol \Rightarrow x + y = 0,15 \\ 100x + 84y = 14,52 \\ \Rightarrow x = 0,12 ; \ y = 0,03 \\ \Rightarrow m = 0,12 . (39 + 35,5) = 8,94 \ g\)
3.2. Bài tập Tính chất của kim loại kiềm, kim loại kiềm thổ và hợp chất của chúng - Nâng cao
Bài 1:
Hấp thụ hoàn toàn 3,36 lít khí CO2 (đktc) vào dung dịch chứa 0,15 mol NaOH và 0,1 mol Ba(OH)2, thu được m gam kết tủa. Giá trị của m là:
Hướng dẫn:
Dạng toán CO2 tác dụng với hỗn hợp bazơ của kim loại nhóm kiềm – kiềm thổ.
\(\begin{array}{l} {n_{C{O_2}}} = \frac{{3,36}}{{22,4}} = 0,15(mol)\\ {n_{O{H^ - }}} = {n_{NaOH}} + 2.{n_{Ba{{(OH)}_2}}} = 0,15 + 2.0,1 = 0,25(mol) \end{array}\)
Vì:\({n_{C{O_2}}}
\({n_{HC{O_3}^ - }} = {n_{C{O_2}}} - {n_{C{O_3}^{2 - }}}\)
\(\Rightarrow {n_{C{O_3}^{2 - }}} = 0,15mol\); có \({n_{Ba{{\left( {OH} \right)}_2}}} = 0,1mol\)
\({n_{BaC{{\rm{O}}_3}}} = 0,1mol\)
Vậy \({m_{BaC{O_3}}} = 19,700g\)
Bài 2:
Hỗn hợp X gồm Na, Ba, Na2O và BaO. Hòa tan hoàn toàn 131,4 gam X vào nước, thu được 6,72 lít khí H2 (đktc) và dung dịch Y, trong đó có 123,12 gam Ba(OH)2. Hấp thụ hoàn toàn 40,32 lít khí CO2 (đktc) vào Y, thu được m gam kết tủa. Giá trị của m là:
Hướng dẫn:
Quy hỗn hợp X về Ba, Na và O.
\({{\rm{n}}_{{\rm{Ba}}}}{\rm{ = }}{{\rm{n}}_{{\rm{Ba(OH}}{{\rm{)}}_{\rm{2}}}}}{\rm{ = 0,72 mol; }}{{\rm{n}}_{{{\rm{H}}_{\rm{2}}}}}{\rm{ = 0,3 mol}}\)
Đặt nNa = x (mol) , nO = y (mol)
BTKL: mNa + mO = mX - mBa ⇔ 23x + 16y = 32,76 (1)
BT electron: ne nhường = ne nhận
(ở đây Na, Ba nhường e, O nhận e về O2-, H+ nhận e thành H2 bay lên)
⇔ x + 2 .0,72 = 2y + 0,3. 2 (2)
Từ (1) và (2) ta có hệ phương trình:
\(\left\{ \begin{array}{l} 23x{\rm{ }} + {\rm{ }}16y{\rm{ }} = {\rm{ }}32,76\;\;\\ x{\rm{ - 2y }} = - 0,84 \end{array} \right. \Leftrightarrow \left\{ \begin{array}{l} x = 0,84\\ y = 0,84 \end{array} \right.\)
⇒ nOH- = nNa + 2nBa = 2,28 mol
\(n_{CO_2}=1,8\ mol\)
\(\Rightarrow n_{{CO_3}^{2-}}=0,48\ mol,\ n_{{HCO_3}^-}=1,32\ mol\)
\(\Rightarrow n_{BaCO_3}=0,48\ mol \Rightarrow m_{BaCO_3}=94,56\ g\)
4. Luyện tập Bài 28 Hóa học 12
Sau bài học cần nắm:
- Tính chất của kim loại kiềm, kim loại kiềm thổ.
- Kĩ năng giải các bài tập và các dạng toán quan trọng.
4.1. Trắc nghiệm
Bài kiểm tra Trắc nghiệm Hoá học 12 Bài 28 có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
-
- A. 2.
- B. 4.
- C. 3.
- D. 1.
-
- A. HCl
- B. NaOH
- C. H2SO4.
- D. BaCl2.
-
- A. Na
- B. Ba
- C. Ca
- D. Cu
-
- A. (1), (2), (3).
- B. (2); (4).
- C. (2); (4); (6).
- D. (2); (4); (5).
-
- A. Trong dãy kim loại kiềm, đi từ Li đến Cs nhiệt độ nóng chảy giảm dần.
- B. Có thể dùng dung dịch Na2CO3 để làm mềm tất cả các loại nước cứng.
- C. Nhiệt độ nóng chảy và nhiệt độ sôi của kim loại kiềm thổ thấp hơn kim loại kiềm.
- D. Một trong những tác dụng của criolit trong quá trình sản xuất nhôm là làm tăng tính dẫn điện.
-
- A. KNO3
- B. Na2CO3
- C. NaNO3
- D. HNO3
-
- A. HCl.
- B. Na2CO3.
- C. Mg(NO3)2.
- D. NaNO3.
-
- A. KHCO3; Ba(OH)2.
- B. NaHCO3; Ba(OH)2.
- C. NaCl; Ba(HCO3)2.
- D. KCl; Ba(HCO3)2.
Câu 3- Câu 5: Xem thêm phần trắc nghiệm để làm thử Online
4.2. Bài tập SGK và Nâng cao
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hoá học 12 Bài 28.
Bài tập 28.6 trang 66 SBT Hóa học 12
Bài tập 28.7 trang 66 SBT Hóa học 12
Bài tập 28.8 trang 66 SBT Hóa học 12
Bài tập 28.9 trang 67SBT Hóa học 12
Bài tập 28.10 trang 67 SBT Hóa học 12
Bài tập 28.11 trang 67 SBT Hóa học 12
Bài tập 28.12 trang 67 SBT Hóa học 12
Bài tập 28.13 trang 67 SBT Hóa học 12
Bài tập 28.14 trang 67 SBT Hóa học 12
Bài tập 28.15 trang 67 SBT Hóa học 12
Bài tập 28.16 trang 68 SBT Hóa học 12
Bài tập 28.17 trang 68 SBT Hóa học 12
5. Hỏi đáp về Bài 28 Chương 6 Hoá học 12
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa HOC247 thảo luận và trả lời nhé.
Bạn có biết?
Hóa học, một nhánh của khoa học tự nhiên, là ngành nghiên cứu về thành phần, cấu trúc, tính chất, và sự thay đổi của vật chất.Hóa học nói về các nguyên tố, hợp chất, nguyên tử, phân tử, và các phản ứng hóa học xảy ra giữa những thành phần đó.Hóa học đôi khi được gọi là "khoa học trung tâm" vì nó là cầu nối các ngành khoa học tự nhiên khác như vật lý học, địa chất học và sinh học.
Nguồn : Wikipedia - Bách khoa toàn thưTâm sự Lớp 12
Lớp 12 - Năm cuối ở cấp tiểu học, năm học quan trọng nhất trong đời học sinh trải qua bao năm học tập, bao nhiêu kì vọng của người thân xung quanh ta. Những nỗi lo về thi đại học và định hướng tương lai thật là nặng. Hãy tin vào bản thân là mình sẽ làm được rồi tương lai mới chờ đợi các em!
Nguồn : ADMIN :))Copyright © 2021 HOCTAPSGK

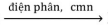 X2 + X3 + H2↑
X2 + X3 + H2↑