Giải Khoa học tự nhiên 7 Bài 6: Giới thiệu về liên kết hóa học giúp các em học sinh lớp 7 nhanh chóng trả lời các câu hỏi SGK Khoa học tự nhiên 7 Kết nối tri thức với cuộc sống trang 36, 37, 38, 39.
Với lời giải Khoa học tự nhiên 7 chi tiết từng phần, từng bài tập, các em dễ dàng ôn tập, củng cố kiến thức Bài 6 Chương II: Phân tử, Liên kết hóa học. Đồng thời, cũng giúp thầy cô tham khảo soạn giáo án cho học sinh của mình. Vậy chi tiết mời thầy cô và các em cùng tham khảo bài viết dưới đây của Download.vn:
Giải KHTN Lớp 7 Bài 6: Giới thiệu về liên kết hóa học
Phần Mở đầu
Trong tự nhiên, chỉ có các khí hiếm tồn tại ở dạng đơn nguyên tử bền vững, còn nguyên tử của các nguyên tố khác thường có xu hướng kết hợp với nhau bằng các liên kết hóa học. Các liên kết hóa học được hình thành như thế nào?
Trả lời:
Nguyên tử của các nguyên tố khác có xu hướng tham gia liên kết hóa học để đạt được lớp electron ngoài cùng giống khí hiếm bằng cách nhường, nhận hay dùng chung các electron.
I. Cấu trúc electron bền vững của khí hiếm
Quan sát Hình 6.1, so sánh số electron lớp ngoài cùng của He, Ne và Ar.
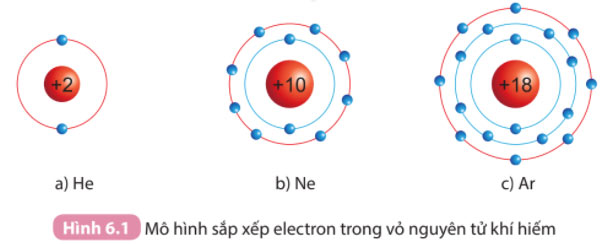
Trả lời:
- He có 2 electron ở lớp vỏ ngoài cùng
- Ne có 8 electron ở lớp vỏ ngoài cùng
- Ar có 8 electron ở lớp vỏ ngoài cùng
=> Nguyên tố He có số electron ở lớp vỏ ngoài cùng ít hơn. Nguyên tố Ne và Ar có số electron ở lớp vỏ ngoài cùng bằng nhau (đều bằng 8).
II. Liên kết ion
Câu 1: Quan sát Hình 6.2 và so sánh số electron ở lớp ngoài cùng của nguyên tử Na, Cl với ion Na+, Cl-.
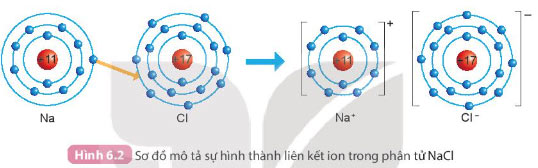
Trả lời:
Số electron lớp ngoài cùng của nguyên tử Na nhiều hơn số electron lớp ngoài cùng của ion Na+
Số electron lớp ngoài cùng của nguyên tử Cl ít hơn số electron lớp ngoài cùng của ion Cl-
Câu 2: Cho sơ đồ mô tả sự hình thành liên kết ion trong phân tử magnesium oxide như sau:
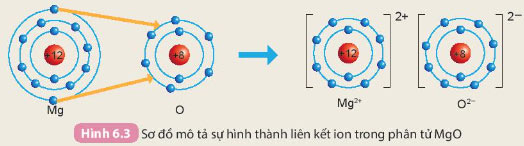
Hãy cho biết nguyên tử Mg đã nhường hay nhận bao nhiêu electron
Trả lời:
Nguyên tử Mg có 12 electron. Ion Mg2+ có tất cả 10 electron
=> Mất đi 2 electron ở lớp vỏ ngoài cùng
=> Nguyên tử Mg đã nhường đi 2 electron ở lớp vỏ ngoài cùng
II. Liên kết cộng hóa trị
1. Liên kết cộng hóa trị trong phân tử đơn chất
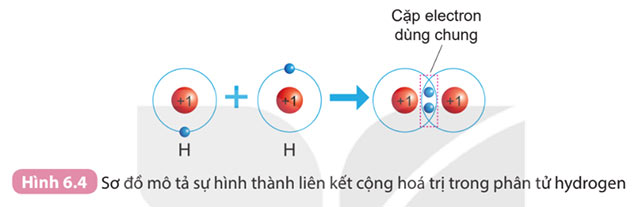
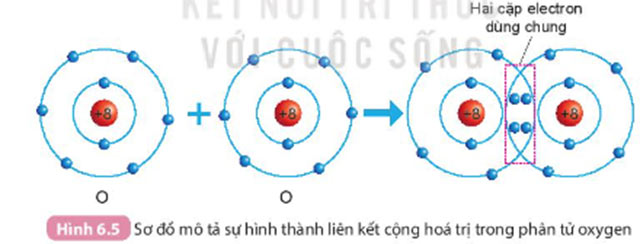
Câu 1. Quan sát Hình 6.4 và Hình 6.5, cho biết số electron lớp ngoài cùng của H và O trước và sau khi tạo thành liên kết cộng hóa trị.
Trả lời:
* Xét Hình 6.4:
- Trước khi tạo thành liên kết cộng hóa trị, H có 1 electron ở lớp vỏ ngoài cùng
- Sau khi tạo thành liên kết cộng hóa trị, H có 2 electron ở lớp vỏ ngoài cùng
* Xét Hình 6.5:
- Trước khi tạo thành liên kết cộng hóa trị, O có 6 electron ở lớp vỏ ngoài cùng (lớp 2)
- Sau khi tạo thành liên kết cộng hóa trị, O có 8 electron ở lớp vỏ ngoài cùng (lớp 2)
Câu 2. Hãy mô tả sự hình thành liên kết cộng hóa trị trong phân tử khí chlorine, khí nitrogen.
Trả lời:
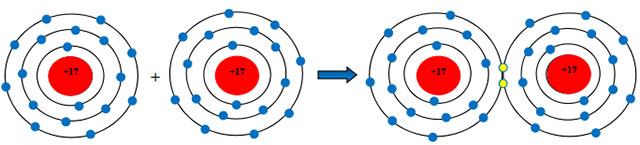
Sự hình thành liên kết cộng hóa trị trong phân tử khí Chlorine
Mỗi nguyên tử Cl có 7 electron ở lớp ngoài cùng. Để có cấu trúc electron bền vững của khí hiếm Ne, khi hình thành phân tử Nitrogen, hai phân tử Cl đã liên kết với nhau bằng cách mỗi nguyên tử N góp chung 1 electron tạo thành 1 cặp electron dùng chung.
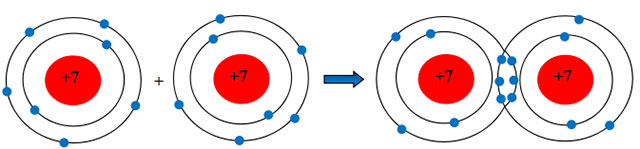
Sự hình thành liên kết cộng hóa trị trong phân tử khí khí Nitrogen
Mỗi nguyên tử N có 5 electron ở lớp ngoài cùng. Để có cấu trúc electron bền vững của khí hiếm Ne, khi hình thành phân tử nitrogen, hai phân tử N đã liên kết với nhau bằng cách mỗi nguyên tử N góp chung 3 electron tạo thành 3 cặp electron dùng chung.
2. Liên kết cộng hóa trị trong phân tử hợp chất
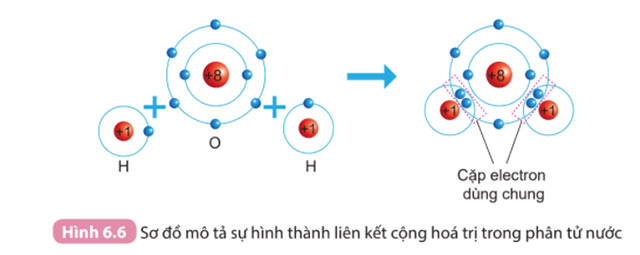
Câu 1. Quan sát Hình 6.6 và cho biết khi nguyên tử O liên kết với hai nguyên tử H theo cách dùng chung electron thì lớp vỏ của nguyên tử oxygen giống với lớp vỏ của nguyên tử khí hiếm nào?
Trả lời:
Khi nguyên tử O liên kết với 2 nguyên tử H bằng cách góp chung electron thì nguyên tử O có 10 electron (2 electron lớp thứ nhất, 8 electron ở lớp thứ 2)
Giống cấu hình electron của khí hiếm Neon (Ne)
Câu 2. Hãy mô tả sự hình thành liên kết cộng hóa trị trong phân tử carbon dioxide, ammonia (gồm một nguyên tử N liên kết với ba nguyên tử H)
Trả lời:
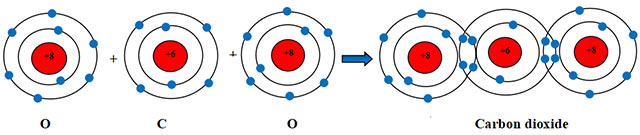
Sự hình thành liên kết cộng hóa trị trong phân tử Carbon Dioxide
Khi hình thành phân tử carbon dioxide, hai nguyên tử O đã liên kết với một nguyên tử C bằng cách nguyên tử C góp chung với mỗi nguyên tử O hai electron tạo thành hai cặp electron dùng chung với mỗi nguyên tử O.
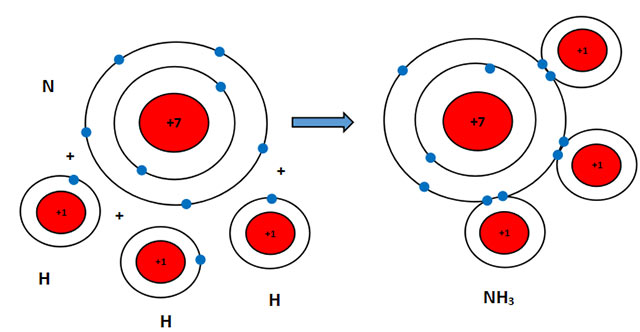
Sự hình thành liên kết cộng hóa trị trong phân tử Ammonia
Khi hình thành phân tử Ammonia, ba nguyên tử H đã liên kết với một nguyên tử N bằng cách nguyên tử N góp chung với mỗi nguyên tử H một electron tạo thành cặp electron dùng chung.
Em có thể?
Vận dụng khái niệm liên kết hóa học để giải thích được vì sao trong tự nhiên, muối ăn ở dạng rắn, khó nóng chảy, khó bay hơi, còn đường ăn, nước đá ở thể rắn dễ nóng chảy và nước ở thể lỏng dễ bay hơi.
Trả lời:
- Muối ăn là hợp chất ion nên là chất rắn ở điều kiện thường, khó bay hơi, khó nóng chảy.
- Đường ăn và nước đá là hợp chất cộng hóa trị nên ở thể rắn, dễ nóng chảy và nước ở thể lỏng sẽ dễ bay hơi do các chất cộng hóa trị thường có nhiệt độ nóng chảy và nhiệt độ sôi thấp.
I. Cấu trúc electron bền vững của khí hiếm
- Ở điều kiện thường, các khí hiếm tồn tại dưới dạng đơn nguyên tử bền vững, khó bị biến đổi hóa học. Lớp electron ngoài cùng của chúng chứa 8 electron (trừ He chứa 2 electron).
ADVERTISING
- Nguyên tử của các nguyên tố khác có xu hướng tham gia liên kết hóa học để đạt được lớp electron ngoài cùng giống khí hiếm bằng cách nhường, nhận hay dùng chung electron.
Lý thuyết KHTN 7 Kết nối tri thức Bài 6: Giới thiệu về liên kết hóa học
II. Liên kết ion
- Nguyên tử trung hòa về điện, khi nguyên tử nhường hay nhận electron, nó trở thành phần tử mang điện gọi là ion.
- Điện tích của ion được viết phía trên, bên phải của kí hiệu hóa học.
- Liên kết ion là liên kết được hình thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
- Sự hình thành liên kết trong phân tử muối ăn (sodium chloride NaCl):
+ Nguyên tử sodium (Na) nhường một electron ở lớp ngoài cùng cho nguyên tử chlorine (Cl) để tạo thành ion dương Na+ có lớp vỏ bền vững giống vỏ nguyên tử khí hiếm Ne.
+ Nguyên tử Cl nhận vào lớp electron ngoài cùng một electron của nguyên tử Na để tạo thành ion âm Cl- có vỏ bền vững giống vỏ nguyên tử khí hiếm Ar.
Lý thuyết Giới thiệu về liên kết hóa học
I. Cấu trúc electron bền vững của khí hiếm
- Ở điều kiện thường, các khí hiếm tồn tại dưới dạng đơn nguyên tử bền vững, khó bị biến đổi hóa học. Lớp electron ngoài cùng của chúng chứa 8 electron (trừ He chứa 2 electron).
- Nguyên tử của các nguyên tố khác có xu hướng tham gia liên kết hóa học để đạt được lớp electron ngoài cùng giống khí hiếm bằng cách nhường, nhận hay dùng chung electron.
II. Liên kết ion
- Nguyên tử trung hòa về điện, khi nguyên tử nhường hay nhận electron, nó trở thành phần tử mang điện gọi là ion.
- Điện tích của ion được viết phía trên, bên phải của kí hiệu hóa học.
- Liên kết ion là liên kết được hình thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
- Sự hình thành liên kết trong phân tử muối ăn (sodium chloride NaCl):
+ Nguyên tử sodium (Na) nhường một electron ở lớp ngoài cùng cho nguyên tử chlorine (Cl) để tạo thành ion dương Na+ có lớp vỏ bền vững giống vỏ nguyên tử khí hiếm Ne.
+ Nguyên tử Cl nhận vào lớp electron ngoài cùng một electron của nguyên tử Na để tạo thành ion âm Cl- có vỏ bền vững giống vỏ nguyên tử khí hiếm Ar.
+ Hai ion được tạo thành mang điện tích trái dấu hút nhau tạo thành liên kết ion trong phân tử muối ăn.
- Chú ý:
+ Khi kim loại tác dụng với phi kim, nguyên tử kim loại nhường electron cho phi kim.
Nguyên tử kim loại trở thành ion dương và nguyên tử phi kim chuyển thành ion âm.
+ Liên kết ion thường được tạo thành giữa kim loại điển hình và phi kim điển hình.
+ Hợp chất ion như muối ăn … là chất rắn ở điều kiện thường, khó bay hơi, khó nóng chảy và khi tan trong nước tạo thành dung dịch dẫn được điện.
III. Liên kết cộng hóa trị
Liên kết cộng hóa trị được tạo nên do sự dùng chung một hay nhiều cặp electron.
1. Liên kết cộng hóa trị trong phân tử đơn chất
a) Sự hình thành phân tử hydrogen
- Mỗi nguyên tử H có một electron ở lớp ngoài cùng.
- Để có cấu trúc electron bền vững của khí hiếm Ne, khi hình thành phân tử hydrogen, hai nguyên tử H đã liên kết với nhau bằng cách mỗi nguyên tử H góp chung 1 electron tạo thành 1 cặp electron dùng chung.
b) Sự hình thành phân tử oxygen
- Mỗi nguyên tử O có 6 electron ở lớp ngoài cùng.
- Để có cấu trúc electron bền vững của khí hiếm Ne, khi hình thành phân tử oxygen, hai nguyên tử O đã liên kết với nhau bằng cách mỗi nguyên tử O góp chung 2 electron để tạo thành 2 cặp electron dùng chung.
Chú ý: Liên kết cộng hóa trị thường gặp nhiều trong phân tử đơn chất phi kim;
2. Liên kết cộng hóa trị trong phân tử hợp chất
Sự hình thành phân tử nước
Khi hình thành phân tử nước, hai nguyên tử H đã liên kết với 1 nguyên tử O bằng cách nguyên tử O góp chung với mỗi nguyên tử H một electron tạo thành cặp electron dùng chung.
Chú ý:
+ Các chất ammonia, carbon dioxide, đường ăn … cũng là các hợp chất cộng hóa trị;
+ Hợp chất cộng hóa trị có thể là chất rắn, chất lỏng hoặc chất khí;
+ Các chất cộng hóa trị thường có nhiệt độ nóng chảy và nhiệt độ sôi thấp.
