Trắc nghiệm tổng hợp Hóa 9 có đáp án !!
Câu hỏi 9 :
Dựa vào tính chất vật lí và hóa học của các chất, hãy phân biệt các chất sau:
a. Bột sắt và bột lưu huỳnh.
Dựa vào tính chất vật lí và hóa học của các chất, hãy phân biệt các chất sau:
a. Bột sắt và bột lưu huỳnh.
Câu hỏi 15 :
Vì sao nói: không khí, nước đường là những hỗn hợp? Có thể thay đổi độ ngọt của đường bằng cách nào?
Câu hỏi 23 :
Viết CTHH của các hợp chất sau:
a. Vôi sống (canxi oxit) biết trong phân tử có một nguyên tử Ca và một nguyên tử O.
Viết CTHH của các hợp chất sau:
a. Vôi sống (canxi oxit) biết trong phân tử có một nguyên tử Ca và một nguyên tử O.
Câu hỏi 28 :
Mol là gì?
a. Một mol nguyên tử gồm bao nhiêu nguyên tử? Lấy ví dụ 1 mol N; 1 mol P; 1 mol Ca; 1 mol Fe.
Mol là gì?
a. Một mol nguyên tử gồm bao nhiêu nguyên tử? Lấy ví dụ 1 mol N; 1 mol P; 1 mol Ca; 1 mol Fe.
Câu hỏi 29 :
b. Một mol nguyên tử có bao nhiêu phân tử? Lấy ví dụ với 1 mol N2; 1 mol NaCl; 1 mol CaO; 1 mol CaCO3.
b. Một mol nguyên tử có bao nhiêu phân tử? Lấy ví dụ với 1 mol N2; 1 mol NaCl; 1 mol CaO; 1 mol CaCO3.
Câu hỏi 43 :
Hãy giải thích tại sao:
a. Khi nung nóng canxi cacbonat (đá vôi) thấy khối lượng giảm đi.
Hãy giải thích tại sao:
a. Khi nung nóng canxi cacbonat (đá vôi) thấy khối lượng giảm đi.
Câu hỏi 45 :
a. Để đốt cháy m gam chất X cần dùng 4,48 lít O2 (ở đktc) thu được 2,24 lít CO2 (đktc) và 2,6 gam H2O. Tính m.
a. Để đốt cháy m gam chất X cần dùng 4,48 lít O2 (ở đktc) thu được 2,24 lít CO2 (đktc) và 2,6 gam H2O. Tính m.
Câu hỏi 55 :
Tính % khối lượng của các nguyên tố có trong các hợp chất sau:
H2O; H2SO4; C2H5OH; CH3−COOH; CnH2n+2; FexOy
Tính % khối lượng của các nguyên tố có trong các hợp chất sau:
H2O; H2SO4; C2H5OH; CH3−COOH; CnH2n+2; FexOyCâu hỏi 60 :
Nếu dùng 11,2g Fe và 3,2g S thì sau phản ứng sẽ thu được những chất nào và với khối lượng là bao nhiêu?
Câu hỏi 68 :
c. Chất X chứa 40% cacbon, 6,67% hiđro và 53,35% oxi. Biết mỗi phân tử Z có 2 nguyên tử oxi.
c. Chất X chứa 40% cacbon, 6,67% hiđro và 53,35% oxi. Biết mỗi phân tử Z có 2 nguyên tử oxi.
Câu hỏi 80 :
Hòa tan 14g vôi sống chứa 20% tạp chất vào một lượng nước dư. Tính khối lượng chất tạo thành sau phản ứng.
Câu hỏi 82 :
Dùng chữ số, công thức hóa học và kí hiệu hóa học để diễn đạt các ý sau:
a. Hai phân tử nước.
Dùng chữ số, công thức hóa học và kí hiệu hóa học để diễn đạt các ý sau:
a. Hai phân tử nước.
Câu hỏi 89 :
b. Đem phân hủy hoàn toàn lượng hợp chất trên thì thu được bao nhiêu lít khí sau phản ứng (đo ở đktc).
b. Đem phân hủy hoàn toàn lượng hợp chất trên thì thu được bao nhiêu lít khí sau phản ứng (đo ở đktc).
Câu hỏi 94 :
Trong những chất dùng làm phân hóa học (phân đạm) sau đây, chất nào có tỉ lệ về khối lượng Nitơ (hàm lượng Nitơ hay hàm lượng đạm) cao nhất?
Trong những chất dùng làm phân hóa học (phân đạm) sau đây, chất nào có tỉ lệ về khối lượng Nitơ (hàm lượng Nitơ hay hàm lượng đạm) cao nhất?
Câu hỏi 98 :
b. Nếu cho thể tích khí thu được ở trên phản ứng hết với khí õi. Tính khối lượng chất lỏng thu được sau phản ứng.
b. Nếu cho thể tích khí thu được ở trên phản ứng hết với khí õi. Tính khối lượng chất lỏng thu được sau phản ứng.
Câu hỏi 102 :
Người ta điều chế kẽm oxi ZnO bằng cách đốt bột kẽm trong oxi.
a. Tính khối lượng oxi cần thiết để điều chế 40,5g kẽm oxit.
Người ta điều chế kẽm oxi ZnO bằng cách đốt bột kẽm trong oxi.
a. Tính khối lượng oxi cần thiết để điều chế 40,5g kẽm oxit.
Câu hỏi 107 :
c. Tính thể tích chất được tạo thành sau phản ứng (biết rằng chất này có thể làm đục nước vôi trong).
c. Tính thể tích chất được tạo thành sau phản ứng (biết rằng chất này có thể làm đục nước vôi trong).
Câu hỏi 109 :
Không khí là một hỗn hợp nhiều chất? Hiện tượng nào chứng tỏ trong không khí
a. Có khí oxi.
Không khí là một hỗn hợp nhiều chất? Hiện tượng nào chứng tỏ trong không khí
a. Có khí oxi.
Câu hỏi 120 :
Tính thể tích khí hiđro (đktc) điều chế được khí cho:
a. 42g sắt tác dụng với axit clohiđric dư.
Tính thể tích khí hiđro (đktc) điều chế được khí cho:
a. 42g sắt tác dụng với axit clohiđric dư.
Câu hỏi 125 :
a. Tính số nguyên tử gam có trong:
- 30g nguyên tố cacbon.
- 80g nguyên tố oxi.
- 40g nguyên tố magie.
a. Tính số nguyên tử gam có trong:
- 30g nguyên tố cacbon.
- 80g nguyên tố oxi.
- 40g nguyên tố magie.
Câu hỏi 126 :
b. Tính số phân tử gam trong:
- 108g nước H2O.
- 8g khí oxi O2.
- 22g khí cacbon.
- 8g đồng (II) oxit CuO.
b. Tính số phân tử gam trong:
- 108g nước H2O.
- 8g khí oxi O2.
- 22g khí cacbon.
- 8g đồng (II) oxit CuO.
Câu hỏi 133 :
Cho 13g kẽm vào một dung dịch chứa 0,5 mol axit clohiđric.
a. Tính thể tích hiđro thu được ở đktc.
Cho 13g kẽm vào một dung dịch chứa 0,5 mol axit clohiđric.
a. Tính thể tích hiđro thu được ở đktc.
Câu hỏi 135 :
Cho phân hủy nước bằng phương pháp điện phân, người ta thu được 28 lít khí oxi (đktc).
a. Viết phương trình phản ứng.
Cho phân hủy nước bằng phương pháp điện phân, người ta thu được 28 lít khí oxi (đktc).
a. Viết phương trình phản ứng.
Câu hỏi 137 :
Khi cho khí hiđro đi qua bột sắt III oxit Fe2O3 nung nóng, người ta thu được sắt theo sơ đồ phản ứng:
Câu hỏi 143 :
a. Dung dịch là gì? Hãy kể vài loại dung môi thường gặp. Cho thí dụ về chất tan là chất rắn, chất lỏng, chất khí.
a. Dung dịch là gì? Hãy kể vài loại dung môi thường gặp. Cho thí dụ về chất tan là chất rắn, chất lỏng, chất khí.
Câu hỏi 145 :
b. Độ tan của một chất là gì? Độ tan phụ thuộc vào yếu tố nào? Thế nào là dung dịch bão hòa, chưa bão hòa?
b. Độ tan của một chất là gì? Độ tan phụ thuộc vào yếu tố nào? Thế nào là dung dịch bão hòa, chưa bão hòa?
Câu hỏi 146 :
Tính nổng độ % của dung dịch thu được khi hòa tan 4,48l khí hiđro clorua (HCl) ở điều kiện tiêu chuẩn vào 500cm3 nước.
Tính nổng độ % của dung dịch thu được khi hòa tan 4,48l khí hiđro clorua (HCl) ở điều kiện tiêu chuẩn vào 500cm3 nước.
Câu hỏi 147 :
Xác định nồng độ % của dung dịch thu được khi hòa tan 25g đồng sunfat ngậm nước (CuSO4.5H2O) vào 175ml nước.
Xác định nồng độ % của dung dịch thu được khi hòa tan 25g đồng sunfat ngậm nước (CuSO4.5H2O) vào 175ml nước.
Câu hỏi 150 :
b. Cô cạn rất từ từ 20ml dung dịch CuSO4 0,2M thu được 10 gam tinh thể CuSO4.yH2O. Tính y.
b. Cô cạn rất từ từ 20ml dung dịch CuSO4 0,2M thu được 10 gam tinh thể CuSO4.yH2O. Tính y.
Câu hỏi 151 :
Hòa tan 60g NaOH vào nước thành 500ml dung dịch. Tìm nồng độ phân tử gam của dung dịch.
Câu hỏi 152 :
Xác định nồng độ phân tử gam của dung dịch thu được khi hòa tan 12,5g CuSO4.5H2O vào 87,5ml nước.
Xác định nồng độ phân tử gam của dung dịch thu được khi hòa tan 12,5g CuSO4.5H2O vào 87,5ml nước.
Câu hỏi 154 :
Phải lấy bao nhiêu ml dung dịch H2SO4 96% (d = 1,84 g/ml) để trong đó có chứa 2,45g H2SO4.
Câu hỏi 157 :
Hòa tan 3,94 gam BaCO3 bằng 500ml dung dịch HCl 0,4M. Cần dùng bao nhiêu ml dung dịch NaOH 0,5M để trung hòa lượng axit dư.
Hòa tan 3,94 gam BaCO3 bằng 500ml dung dịch HCl 0,4M. Cần dùng bao nhiêu ml dung dịch NaOH 0,5M để trung hòa lượng axit dư.
Câu hỏi 158 :
Hòa tan 155g natri oxit vào 145g nước để tạo thành dung dịch có tính kiềm. Tính nồng độ % thu được.
Câu hỏi 159 :
Hòa tan 2,3 gam natri kim loại vào 197,8 gam nước.
a. Tính nồng độ % dung dịch thu được.
Hòa tan 2,3 gam natri kim loại vào 197,8 gam nước.
a. Tính nồng độ % dung dịch thu được.
Câu hỏi 160 :
b. Tính nồng độ mol/l dung dịch thu được (dung dịch có khối lượng riêng d = 1,08 g/ml).
b. Tính nồng độ mol/l dung dịch thu được (dung dịch có khối lượng riêng d = 1,08 g/ml).
Câu hỏi 167 :
b. Nồng độ dung dịch bão hòa muối ăn ở 20oC là 26,5%. Tính độ tan của muối ăn ở cùng nhiêt độ.
b. Nồng độ dung dịch bão hòa muối ăn ở 20oC là 26,5%. Tính độ tan của muối ăn ở cùng nhiêt độ.
Câu hỏi 168 :
a. Độ tan của muối ăn ở 20oC là 36g. Xác định nồng độ % của dung dịch bão hòa ở nhiệt độ đó.
a. Độ tan của muối ăn ở 20oC là 36g. Xác định nồng độ % của dung dịch bão hòa ở nhiệt độ đó.
Câu hỏi 170 :
Hòa tan hoàn toàn 4g MgO bằng dung dịch H2SO4 19,6% (vừa đủ). Tính nồng độ % dung dịch muối tạo thành sau phản ứng.
Hòa tan hoàn toàn 4g MgO bằng dung dịch H2SO4 19,6% (vừa đủ). Tính nồng độ % dung dịch muối tạo thành sau phản ứng.
Câu hỏi 171 :
Cần lấy bao nhiêu gam CaCl2.6H2O để khi hòa tan vào được thì thu được 200ml dung dịch canxi clorua 0% (d = 1,28 g/ml)?
Cần lấy bao nhiêu gam CaCl2.6H2O để khi hòa tan vào được thì thu được 200ml dung dịch canxi clorua 0% (d = 1,28 g/ml)?
Câu hỏi 172 :
Tính lượng tinh thể CuSO4. 5H2O cần dùng để điều chế 500ml dung dịch CuSO4 8% (D = 1,1 g/mol).
Tính lượng tinh thể CuSO4. 5H2O cần dùng để điều chế 500ml dung dịch CuSO4 8% (D = 1,1 g/mol).
Câu hỏi 173 :
Để hòa tan 6,3g Zn thì tiêu tốn hết m (g) dung dịch HCl 30%.
a. Tính khối lượng m của dung dịch HCl đã dùng.
Để hòa tan 6,3g Zn thì tiêu tốn hết m (g) dung dịch HCl 30%.
a. Tính khối lượng m của dung dịch HCl đã dùng.
Câu hỏi 175 :
Tính chất nào sau đây cho biết chất đó là tinh khiết:
Câu hỏi 176 :
Chất nào sau đây được coi là tinh khiết?
(1) Nước suối.
(2) Nước cất.
(3) Nước khoáng.
(4) Nước đá sản xuất từ nhà máy.
(5) Nước lọc.
Chất nào sau đây được coi là tinh khiết?
(1) Nước suối.
(2) Nước cất.
(3) Nước khoáng.
(4) Nước đá sản xuất từ nhà máy.
(5) Nước lọc.
Câu hỏi 177 :
Có một chất lỏng không màu không mùi đựng trong một ống nghiệm. Nhúng ống nghiệm này vào cốc thủy tinh đựng nước sôi, nhận thấy chất lỏng sôi ngay. Dự đoán nào về nhiệt độ sôi của chất lỏng là đúng nhất?
Câu hỏi 178 :
Phép lọc được dùng để tách một hỗn hợp gồm:
Câu hỏi 179 :
Phép chưng cất được dùng để tách một hỗn hợp gồm:
Phép chưng cất được dùng để tách một hỗn hợp gồm:
Câu hỏi 180 :
Có thể thay đổi độ ngọt của đường bằng cách:
Câu hỏi 181 :
Cho các nguyên tử với các thành phần cấu tạo sau:
X (6n; 5p; 5e)
Y (10p; 10p; 10n)
Z (5e; 5p; 5n)
T (11p; 11e; 12n)
Ở đây có bao nhiêu nguyên tố hóa học?
Cho các nguyên tử với các thành phần cấu tạo sau:
X (6n; 5p; 5e)
Y (10p; 10p; 10n)
Z (5e; 5p; 5n)
T (11p; 11e; 12n)
Ở đây có bao nhiêu nguyên tố hóa học?
D. 4
B. 3
C. 2
D. 1
Câu hỏi 182 :
Dãy chất nào dưới đây gồm toàn kim loại?
Câu hỏi 183 :
Cho dãy kí hiệu các nguyên tố sau: O, Ca, N, Fe, S.
Theo thứ tự tên các nguyên tố lần lượt là:
Cho dãy kí hiệu các nguyên tố sau: O, Ca, N, Fe, S.
Theo thứ tự tên các nguyên tố lần lượt là:
Câu hỏi 184 :
Trong số các chất dưới đây, thuộc loại đơn chất có:
Câu hỏi 185 :
Trong số các chất dưới đây, thuộc loại hợp chất có:
Câu hỏi 186 :
Phương pháp thích hợp nhất để tách được muối ăn từ nước biển:
Câu hỏi 187 :
Câu sau đây gồm hai phần: “ Nước cất là một hợp chất vì nước cất sôi ở đúng 100oC”.
Hãy chọn phương án đúng trong số các phương án sau:
Câu sau đây gồm hai phần: “ Nước cất là một hợp chất vì nước cất sôi ở đúng 100oC”.
Hãy chọn phương án đúng trong số các phương án sau:
Câu hỏi 189 :
Từ công thức hóa học Na2CO3 cho biết ý nào đúng:
(1) Hợp chất trên do 3 đơn chất Na, C, O tạo nên.
(2) Hợp chất trên do 3 nguyên tố Na, C, O tạo nên.
(3) Hợp chất trên có PTK = 23 + 12 + 16 = 51.
(4) Hợp chất trên có PTK = .
Từ công thức hóa học Na2CO3 cho biết ý nào đúng:
(1) Hợp chất trên do 3 đơn chất Na, C, O tạo nên.
(2) Hợp chất trên do 3 nguyên tố Na, C, O tạo nên.
(3) Hợp chất trên có PTK = 23 + 12 + 16 = 51.
(4) Hợp chất trên có PTK = .
Câu hỏi 190 :
Trong các công thức hóa học sau, công thức hóa hoạc nào là của hợp chất:
(1) CH4, K2SO4, Cl2, O3, NH3.
(2) O2, CO2, CaO, N2, H2O2.
(3) H2O, Ca(HCO3)2, Fe(OH)3, CuSO4.
(4) Br2, HBr, CO, Hg, Ni.
(5) PbO, HI, HNO3, Cr2O3, NO.
Trong các công thức hóa học sau, công thức hóa hoạc nào là của hợp chất:
(1) CH4, K2SO4, Cl2, O3, NH3.
(2) O2, CO2, CaO, N2, H2O2.
(3) H2O, Ca(HCO3)2, Fe(OH)3, CuSO4.
(4) Br2, HBr, CO, Hg, Ni.
(5) PbO, HI, HNO3, Cr2O3, NO.
Câu hỏi 191 :
Trong các cách viết công thức hóa học sau, cách viết nào đúng:
(1) CH4; H2O2; O3; Ca(OH)2; MgO.
(2) CO; Fe2O2; CuO2; Hg2O; Ag2O.
(3) N2; N2O2; CH3; Cu3(SO4)2; Zn(OH)2.
(4) Fe3O4; Mg(OH)2Cl; Ca(HCO3)2; NaAlO2.
(5) Cr2O; AgOH; NaCl2; K2O; Al2O3.
Trong các cách viết công thức hóa học sau, cách viết nào đúng:
(1) CH4; H2O2; O3; Ca(OH)2; MgO.
(2) CO; Fe2O2; CuO2; Hg2O; Ag2O.
(3) N2; N2O2; CH3; Cu3(SO4)2; Zn(OH)2.
(4) Fe3O4; Mg(OH)2Cl; Ca(HCO3)2; NaAlO2.
(5) Cr2O; AgOH; NaCl2; K2O; Al2O3.
Câu hỏi 192 :
Cho biết công thức hóa học hợp chất của nguyên tố X với O và hợp chất của nguyên tố Y với H như (X, Y là những nguyên tố nào đó): XO; TH3. Hãy chọn công thức hóa học đúng cho hợp chất của X và Y trong các công thức sau đây:
Câu hỏi 193 :
Theo hóa trị của sắt, trong hợp chất có công thức hóa học là Fe2O3, hãy chọn công thức hóa học đúng trong số các công thức hợp chất có phân tử gồm Fe liên kết với (SO4) hóa trị (II) sai:
Câu hỏi 194 :
Cho các chất sau: Cl2; H2SO4; Cu(NO3)2; Al2(SO4)3.
Khối lượng phân tử khối lần lượt là:
Cho các chất sau: Cl2; H2SO4; Cu(NO3)2; Al2(SO4)3.
Khối lượng phân tử khối lần lượt là:
Câu hỏi 195 :
Phân tử khí ozon gồm ba nguyên tử oxi. Công thức hóa học của ozon là:
Câu hỏi 197 :
Phát biểu nào sau đây là sai:
Câu hỏi 198 :
Một hợp chất X có thành phần gồm 2 nguyên tố C và O. Biết tỉ lệ khối lượng của C đối với O là mC : mO = 3 : 8. Công thức phân tử của X là:
Câu hỏi 199 :
Một hợp chất Y có phân tử khối là 58 đvc, cấu tạo từ 2 nguyên tố C và H trong đó C chiếm 82,76% khối lượng của hợp chất. Công thức phân tử của Y là:
Câu hỏi 200 :
Các hiện tượng sau đây, hiện tam giác nào có sự biến đổi hóa học?
a. Sắt được cắt nhỏ thành từng đoạn và tán thành đinh.
b. Vành xa đạp bằng sắt bị phủ một lớp gỉ là chất màu nâu đỏ.
c. Rượu để lâu trong không khí thường bị chua.
d. Đèn tín hiệu chuyển từ màu xanh sang màu đỏ.
e. Dây tóc trong bóng đèn điện nóng và sáng lên khi dòng điện chạy qua.
Các hiện tượng sau đây, hiện tam giác nào có sự biến đổi hóa học?
a. Sắt được cắt nhỏ thành từng đoạn và tán thành đinh.
b. Vành xa đạp bằng sắt bị phủ một lớp gỉ là chất màu nâu đỏ.
c. Rượu để lâu trong không khí thường bị chua.
d. Đèn tín hiệu chuyển từ màu xanh sang màu đỏ.
e. Dây tóc trong bóng đèn điện nóng và sáng lên khi dòng điện chạy qua.
Câu hỏi 201 :
Những hiện tượng sau, hiện tượng nào là hiện tượng hóa học?
a. Về mùa hè thức ăn thường bị thiu.
b. Đun đường, đường ngả màu nâu rồi đen đi.
c. Các quả bóng bay trên trời rồi nổ tung.
d. Cháy rừng gây ô nhiễm lớn cho môi trường.
e. Nhiệt độ Trái đất nóng lên làm băng ở hai cực Trái đất tan dần.
Những hiện tượng sau, hiện tượng nào là hiện tượng hóa học?
a. Về mùa hè thức ăn thường bị thiu.
b. Đun đường, đường ngả màu nâu rồi đen đi.
c. Các quả bóng bay trên trời rồi nổ tung.
d. Cháy rừng gây ô nhiễm lớn cho môi trường.
e. Nhiệt độ Trái đất nóng lên làm băng ở hai cực Trái đất tan dần.
Câu hỏi 202 :
Trong số những quá trình và sự việc dưới đây, đâu là hiện tượng vật lí:
a. Hòa tan muối ăn vào nước ta được dung dịch muối ăn.
b. Có thể lặp lại thí nghiệm với chất vừa dùng để làm thí nghiệm trước đó.
c. Cồn để trong lọ không kín bị bay hơi.
d. Nước bị đóng băng ở hai cực Trái đất.
e. Cho vôi sống CaO hòa tan vào nước.
Trong số những quá trình và sự việc dưới đây, đâu là hiện tượng vật lí:
a. Hòa tan muối ăn vào nước ta được dung dịch muối ăn.
b. Có thể lặp lại thí nghiệm với chất vừa dùng để làm thí nghiệm trước đó.
c. Cồn để trong lọ không kín bị bay hơi.
d. Nước bị đóng băng ở hai cực Trái đất.
e. Cho vôi sống CaO hòa tan vào nước.
Câu hỏi 215 :
Có 4 gói bột oxit màu đen tương tự nhau: CuO, MnO2, AgO và FeO. Chỉ dùng dung dịch HCl có thể nhận biết được những oxit nào?
Có 4 gói bột oxit màu đen tương tự nhau: CuO, MnO2, AgO và FeO. Chỉ dùng dung dịch HCl có thể nhận biết được những oxit nào?
Câu hỏi 216 :
Có 3 chất là Mg, Al, Al2O3. Chỉ được dùng một hóa chất làm thuốc thử phân biệt ba chất trên. Viết phương trình phản ứng.
Có 3 chất là Mg, Al, Al2O3. Chỉ được dùng một hóa chất làm thuốc thử phân biệt ba chất trên. Viết phương trình phản ứng.
Câu hỏi 219 :
Định nghĩa và phân loại axit.
a. Hãy nêu phương pháp chính để điều chế axit. Cho các thí dụ minh họa.
Định nghĩa và phân loại axit.
a. Hãy nêu phương pháp chính để điều chế axit. Cho các thí dụ minh họa.
Câu hỏi 223 :
Cho biết nhôm hiđroxit là hợp chất lưỡng tính, viết các phương trình phản ứng của nhôm hiđroxit với các dung dịch HCl và NaOH.
Cho biết nhôm hiđroxit là hợp chất lưỡng tính, viết các phương trình phản ứng của nhôm hiđroxit với các dung dịch HCl và NaOH.
Câu hỏi 224 :
a. Phản ứng nào đặc trưng cho oxit bazơ, phản ứng nào chỉ đặc trưng cho oxit bazơ kiềm?
a. Phản ứng nào đặc trưng cho oxit bazơ, phản ứng nào chỉ đặc trưng cho oxit bazơ kiềm?
Câu hỏi 239 :
Hòa tan 15,5g Na2O vào nước tạo thành 0,5 lít dung dịch.
a. Tính nồng độ mol/l của dung dịch thu được.
Hòa tan 15,5g Na2O vào nước tạo thành 0,5 lít dung dịch.
a. Tính nồng độ mol/l của dung dịch thu được.
Câu hỏi 243 :
Cho 9,4g K2O vào nước. Tính khối lượng SO2 cần thiết phản ứng với dung dịch trên để tạo thành:
a. Muối trung hòa.
Cho 9,4g K2O vào nước. Tính khối lượng SO2 cần thiết phản ứng với dung dịch trên để tạo thành:
a. Muối trung hòa.
Câu hỏi 244 :
Cho 9,4g K2O vào nước. Tính khối lượng SO2 cần thiết phản ứng với dung dịch trên để tạo thành:
b. Muối axit.
Cho 9,4g K2O vào nước. Tính khối lượng SO2 cần thiết phản ứng với dung dịch trên để tạo thành:
b. Muối axit.
Câu hỏi 245 :
Phản ứng của nguyên tố X với nguyên tố Y được biểu diễn trong sơ đồ dưới đây (nguyên tử X, Y kí hiệu lần lượt là (O) và ).
Phương trình nào dưới đây biểu diễn tốt nhất phản ứng này:
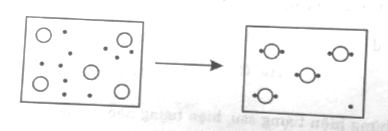
Phản ứng của nguyên tố X với nguyên tố Y được biểu diễn trong sơ đồ dưới đây (nguyên tử X, Y kí hiệu lần lượt là (O) và ).
Phương trình nào dưới đây biểu diễn tốt nhất phản ứng này:

A.
B.
C.
D.
Câu hỏi 247 :
Phân tích một khối lượng hợp chất M, người ta nhận thấy thành phần khối lượng của nó có 50% là lưu huỳnh và 50% là oxi. Công thức của hợp chất M có thể là:
Câu hỏi 249 :
Một hợp chất X có thành phần gồm 2 nguyên tố C và O. Biết tỉ lệ về khối lượng của C đối với O là mC : mO = 3 : 8. X có công thức phân tử là công thức nào sau đây?
Câu hỏi 250 :
Cho biết công thức hóa học hợp chất của nguyên tố X với H và hợp chất Y với Cl như sau: XH2; YCl3. Hãy chọn công thức thích hợp cho hợp chất của X và Y trong số các công thức sau đây:
Câu hỏi 252 :
Oxit của một nguyên tố hóa học có hóa trị II chứa 20% oxi (về khối lượng). Oxit có công thức hóa học là:
Câu hỏi 253 :
Oxit nào giàu oxi nhất (hàm lượng % oxi lớn nhất)?
Câu hỏi 254 :
Quặng nào giàu sắt nhất?
Câu hỏi 256 :
Hai nguyên tử Y kết hợp với ba nguyên tử O tạo ra phân tử oxit. Trong phân tử oxit, oxi chiếm 30% về khối lượng. Đó là nguyên tố kim loại nào sau đây?
A. Ca
B. Fe
C. Cu
D. Zn
Câu hỏi 257 :
Một hợp chất hữu cơ có nguyên tố cacbon chiếm 80% và 20% là hiđro. Tỉ khối của hợp chất với hiđro bằng 15. Công thức hóa học của hợp chất hữu cơ là:
Câu hỏi 259 :
Một loại quặng sắt chứa 90% Fe3O4. Khối lượng sắt có trong một tấn quặng đó là:
Một loại quặng sắt chứa 90% Fe3O4. Khối lượng sắt có trong một tấn quặng đó là:
Câu hỏi 260 :
Phát biểu nào dưới đây là đúng:
Câu hỏi 261 :
8,8g khí cacbonic có cùng số mol phân tử với:
Câu hỏi 263 :
Cần lấy bao nhiêu gam oxi để có số phân tử bằng nửa số phân tử có trong 22g CO2?
Câu hỏi 264 :
Cho tỉ khối của khí A đối với khí B là 2,125 và tỉ khối của khí B đối với oxi là 0,5. Khối lượng mol của khí A là:
Câu hỏi 265 :
Cho biết 400cm3 một chất khí ở đktc có khối lượng 1,143g. Khối lượng mol phân tử của chất khí đó là:
Cho biết 400cm3 một chất khí ở đktc có khối lượng 1,143g. Khối lượng mol phân tử của chất khí đó là:
Câu hỏi 267 :
Cho các chất sau:
a. Fe3O4.
b. KClO3.
c. KMnO4.
d. CaCO3.
e. Không khí.
g. H2O.
Những chất được dùng để điều chế oxi trong phòng thí nghiệm là:
Cho các chất sau:
a. Fe3O4.
b. KClO3.
c. KMnO4.
d. CaCO3.
e. Không khí.
g. H2O.
Những chất được dùng để điều chế oxi trong phòng thí nghiệm là:
Câu hỏi 268 :
Người ta thu khĩ oxi bằng cách đẩy nước là nhờ dựa vào tính chất:
Câu hỏi 269 :
Người ta còn thu khí oxi bằng cách đẩy không khí là nhờ dựa vào tính chất:
Người ta còn thu khí oxi bằng cách đẩy không khí là nhờ dựa vào tính chất:
Câu hỏi 270 :
Sự oxi hóa chậm là:
Câu hỏi 271 :
c. Tính thể tích CO2 (đktc) trong trường hợp chỉ tạo ra muối không tan. Tính khối lượng muối không tan đó.
c. Tính thể tích CO2 (đktc) trong trường hợp chỉ tạo ra muối không tan. Tính khối lượng muối không tan đó.
Câu hỏi 272 :
Khi phân hủy có xúc tác 122,5g kali clorat KClO3, thể tích khí oxi thu được là:
Khi phân hủy có xúc tác 122,5g kali clorat KClO3, thể tích khí oxi thu được là:
Câu hỏi 275 :
Số gam kali pemanganat KMnO4 cần dùng để điều chế được 2,24l khí oxi (đktc) là:
Số gam kali pemanganat KMnO4 cần dùng để điều chế được 2,24l khí oxi (đktc) là:
Câu hỏi 276 :
Trong các oxit sau đây: SO3, CuO, Na2O, CaO, CO2, Al2O3, oxit nào tác dụng được với nước?
Câu hỏi 277 :
Sau khi nung 8g một hỗn hợp kẽm cacbonat và kẽm oxit, người ta thu được 6,24g ZnO.
a. Tính % khối lượng hỗn hợp ban đầu.
Sau khi nung 8g một hỗn hợp kẽm cacbonat và kẽm oxit, người ta thu được 6,24g ZnO.
a. Tính % khối lượng hỗn hợp ban đầu.
Câu hỏi 278 :
Cho những oxit sau: SO2, K2O, Li2O, CaO, MgO, CO, NO, N2O5, P2O5. Những oxit vừa tác dụng với nước, vừa tác dụng với axit là:
Câu hỏi 280 :
Có 3 oxit sau: MgO, SO3, Na2O. Có thể nhận biết được các chất đó bằng thuốc thử sau đây không?
Câu hỏi 282 :
Khu mỏ sắt ở Trại Cau (Thái Nguyên) có một loại quặng sắt. Khi phân tích một mẫu quặng này, người ta nhận thấy có 2,8g sắt. Trong mẫu quặng trên, khối lượng sắt (III) oxit Fe2O3 ứng với hàm lượng sắt nói trên là:
Câu hỏi 284 :
Tỉ lệ khối lượng của nitơ và oxi trong một oxit là 7 : 20. Công thức của oxit là:
Tỉ lệ khối lượng của nitơ và oxi trong một oxit là 7 : 20. Công thức của oxit là:
Câu hỏi 285 :
Cho 28,4g đi photpho pentaoxit P2O5 vào cốc chứa 90g H2O để tạo thành axit photphoric H3PO4. Khối lượng axit H3PO4 tạo thành là:
Câu hỏi 287 :
Cho các oxit có công thức hóa học sau: CO2, CO, Mn2O7, SiO2, P2O5, NO2, N2O5, CaO, Al2O3. Các oxit axit được sắp xếp như sau:
Câu hỏi 288 :
Có 4 lọ đựng riêng biệt: nước cất, dung dịch axx sunfuric H2SO4, dung dịch natri hiđroxit NaOH, dung dịch muối ăn NaCl. Bằng cách nào có thể nhận biết được mỗi chất trong các lọ?
Câu hỏi 289 :
Tính lượng axit sunfuric thu được từ 60kg quặng pirit nếu hiệu suất phản ứng là 85% so với lí thuyết.
Tính lượng axit sunfuric thu được từ 60kg quặng pirit nếu hiệu suất phản ứng là 85% so với lí thuyết.
Câu hỏi 290 :
Có 4 lọ mất nhãn đựng 4 chất bột màu trắng gồm: CaO, Na2O, MgO và P2O5. Dùng thuốc thử nào để nhận biết các chất trên?
Câu hỏi 291 :
Hòa tan 3,1g Na2O vào nước để được 2 lít dung dịch
a. Cho biết nồng độ M của dung dịch thu được.
Hòa tan 3,1g Na2O vào nước để được 2 lít dung dịch
a. Cho biết nồng độ M của dung dịch thu được.
Câu hỏi 292 :
Cho 11,2g sắt tác dụng với dung dịch axit sunfuric loãng có chứa 12,25g H2SO4. Thể tích H2 (đktc) thu được là:
Câu hỏi 295 :
c. Tính nồng độ phân tử gam của muối tạo thành sau phản ứng. Biết rằng dung dịch H2SO4 20% có khối lượng riêng 1,14 g/ml.
c. Tính nồng độ phân tử gam của muối tạo thành sau phản ứng. Biết rằng dung dịch H2SO4 20% có khối lượng riêng 1,14 g/ml.
Câu hỏi 296 :
Bột nhôm cháy theo phản ứng: Nhôm + khí oxi Nhôm oxit (Al2O3)
Cho biết khối lượng nhôm đã phản ứng là 54g và khối lượng nhôm oxit sinh ra là 102g. Vậy thể tích oxi đã dùng là thể tích nào dưới đây?
Bột nhôm cháy theo phản ứng: Nhôm + khí oxi Nhôm oxit (Al2O3)
Cho biết khối lượng nhôm đã phản ứng là 54g và khối lượng nhôm oxit sinh ra là 102g. Vậy thể tích oxi đã dùng là thể tích nào dưới đây?
Câu hỏi 297 :
Khi đốt cháy 1 mol chất Y cần 6,5 mol O2 và thu được 4 mol CO2 và 5 mol H2O. Chất Y có công thức phân tử nào sau đây:
Câu hỏi 298 :
Cho 11g dung dịch H2SO4 20% vào 400g dung dịch BaCl2 5,2%.
a. Viết phương trình phản ứng và tính khối lượng kết tủa tạo thành.
Cho 11g dung dịch H2SO4 20% vào 400g dung dịch BaCl2 5,2%.
a. Viết phương trình phản ứng và tính khối lượng kết tủa tạo thành.
Câu hỏi 299 :
Trong giờ thực hành thí nghiệm, một học sinh đốt cháy 3,2 gam lưu huỳnh trong 1,12 lít oxi (đktc). Sau phản ứng sẽ có:
Câu hỏi 302 :
Người ta điều chế vôi sống (CaO) bằng cách nung đá vôi (CaCO3). Lượng vôi sống thu được từ 1 tấn đá vôi có chứa 10% tạp chất là 0,45 tấn. Hiệu suất phản ứng là:
Câu hỏi 305 :
Trong các phản ứng hóa học sau, phản ứng nào là phản ứng hóa hợp, phản ứng phân hủy, phản ứng oxi hóa khử, phản ứng thế?
Trong các phản ứng hóa học sau, phản ứng nào là phản ứng hóa hợp, phản ứng phân hủy, phản ứng oxi hóa khử, phản ứng thế?
Câu hỏi 307 :
Trong các phản ứng hóa học sau, phản ứng nào là phản ứng phân hủy?
Trong các phản ứng hóa học sau, phản ứng nào là phản ứng phân hủy?
Câu hỏi 308 :
c. Tính nồng độ mol/l của chất còn lại trong dung dịch. Cho rằng thể tích dung dịch sau phản ứng thay đổi không đáng kể.
c. Tính nồng độ mol/l của chất còn lại trong dung dịch. Cho rằng thể tích dung dịch sau phản ứng thay đổi không đáng kể.
Câu hỏi 309 :
Trong các phản ứng hóa học sau, phản ứng nào là phản phản ứng thế?
Câu hỏi 312 :
b. Từ lượng axit sunfuric này người ta có thể pha chế được bao nhiêu tấn dung dịch H2SO4 23%.
b. Từ lượng axit sunfuric này người ta có thể pha chế được bao nhiêu tấn dung dịch H2SO4 23%.
Câu hỏi 314 :
Để hòa tan 2,4g oxit một kim loại hóa trị II cần dùng 2,19g axit HCl. Hỏi đó là oxit kim loại nào?
Để hòa tan 2,4g oxit một kim loại hóa trị II cần dùng 2,19g axit HCl. Hỏi đó là oxit kim loại nào?
Câu hỏi 316 :
Trong các phản ứng hóa học sau phản ứng oxi - hóa khử là?
Câu hỏi 320 :
Cho sơ đồ phản ứng với các đặc điểm được ghi rõ như sau:
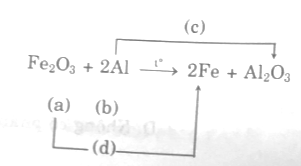
Cho biết phát biểu nào dưới đây là đúng:
Cho sơ đồ phản ứng với các đặc điểm được ghi rõ như sau:

Cho biết phát biểu nào dưới đây là đúng:
Câu hỏi 325 :
Cần dùng bao nhiêu lít dung dịch NaOH 0,5M để trung hòa 250ml dung dịch X chứa axit HCl 2M và H2SO4 1,5M.
Cần dùng bao nhiêu lít dung dịch NaOH 0,5M để trung hòa 250ml dung dịch X chứa axit HCl 2M và H2SO4 1,5M.
Câu hỏi 326 :
Các phương trình phản ứng sau, phản ứng nào là phản ứng oxi hóa khử?
Các phương trình phản ứng sau, phản ứng nào là phản ứng oxi hóa khử?
Câu hỏi 327 :
Những oxit sau: SO2, CO2, CO, CaO, MgO, CuO, Na2O, Al2O3, N2O5, K2O. Những oxit nào vừa tác dụng được với nước, vừa tác dụng được với axit hoặc vừa tác dụng được với nước, vừa tác dụng được với kiềm?
Câu hỏi 329 :
Cho CuO tác dụng với dung dịch axit HCl sẽ có hiện tượng sau:
Câu hỏi 330 :
Trong số những chất có công thức hóa học dưới đây, chất nào làm quỳ tím hóa đỏ?
Trong số những chất có công thức hóa học dưới đây, chất nào làm quỳ tím hóa đỏ?
Câu hỏi 331 :
Trong phòng thí nghiệm có các kim loại kẽm và magie, các dung dịch axit sunfuric loãng H2SO4 và axit clohiđric HCl. Muốn điều chế được 1,12 lít khí hiđro (đktc) phải dùng kim loại nào, axit nào để chỉ cần một khối lượng nhỏ nhất?
Câu hỏi 333 :
Có những chất rắn sau: CaO, P2O5, MgO, Na2SO4. Dùng những thuốc thử nào để có thể phân biệt được các chất trên?
Câu hỏi 334 :
a. Có 3 gói phân hóa học KCl; NH4NO3 và supe phốt phát. Dựa vào phản ứng đặc trưng nào để phân biệt chúng?
a. Có 3 gói phân hóa học KCl; NH4NO3 và supe phốt phát. Dựa vào phản ứng đặc trưng nào để phân biệt chúng?
Câu hỏi 335 :
Bằng phương pháp hóa học làm thế nào để nhận ra sự có mặt của mỗi khí trong hỗn hợp gồm: CO, CO2, SO3?
Câu hỏi 337 :
Có 6 lọ mất nhãn chứa dung dịch các chất sau: HCl, H2SO4, BaCl2, NaCl, NaOH, Ba(OH)2. Hãy chọn một thuốc thử để nhận biết các dung dịch trên.
Câu hỏi 338 :
Trong số những chất dưới đây, chất nào làm cho quỳ tím hóa xanh?
Câu hỏi 339 :
Trong số những chất có công thức hóa học dưới đây, chất nào làm quỳ tím không đổi màu?
Câu hỏi 340 :
Dãy chất nào chỉ bao gồm toàn axit?
Câu hỏi 341 :
Dãy chất nào chỉ bao gồm toàn muối?
Câu hỏi 343 :
Cho biết phát biểu nào dưới đây là đúng?
Câu hỏi 345 :
Dung dịch là:
Câu hỏi 346 :
Đồng (II) sunfat tan vào nước tạo thành dung dịch có màu xanh lơ. Màu xanh càng đậm nếu nồng độ dung dịch càng cao. Có 4 dung dịch được pha chế như sau (thể tích dung dịch coi bằng thể tích nước).
Dung dịch I: 100ml H2O và 2,4g CuSO4.
Dung dịch II: 300ml H2O và 6,4g CuSO4.
Dung dịch III: 200ml H2O và 3,2g CuSO4.
Dung dịch IV: 400ml H2O và 8,0g CuSO4.
Hỏi: Dung dịch nào có màu xanh đậm nhất?
Đồng (II) sunfat tan vào nước tạo thành dung dịch có màu xanh lơ. Màu xanh càng đậm nếu nồng độ dung dịch càng cao. Có 4 dung dịch được pha chế như sau (thể tích dung dịch coi bằng thể tích nước).
Dung dịch I: 100ml H2O và 2,4g CuSO4.
Dung dịch II: 300ml H2O và 6,4g CuSO4.
Dung dịch III: 200ml H2O và 3,2g CuSO4.
Dung dịch IV: 400ml H2O và 8,0g CuSO4.
Hỏi: Dung dịch nào có màu xanh đậm nhất?
Câu hỏi 347 :
Dung dịch là hỗn hợp
Câu hỏi 348 :
Để hòa tan hoàn toàn 3,6g magie phải dùng bao nhiêu ml dung dịch hỗn hợp HCl 1M và H2SO4 0,75M.
Để hòa tan hoàn toàn 3,6g magie phải dùng bao nhiêu ml dung dịch hỗn hợp HCl 1M và H2SO4 0,75M.
Câu hỏi 349 :
Nồng độ phần trăm của dung dịch là:
Câu hỏi 350 :
Nồng độ mol/l của dung dịch là:
Câu hỏi 351 :
Độ tan của một chất trong nước ở một nhiệt độ xác định là:
Câu hỏi 352 :
Cho 5,6 lít khí CO2 lội qua dung dịch NaOH 20%.
(D = 1,22 g/mol)
a. Tính khối lượng muối tạo thành.
Cho 5,6 lít khí CO2 lội qua dung dịch NaOH 20%.
(D = 1,22 g/mol)
a. Tính khối lượng muối tạo thành.
Câu hỏi 353 :
Lấy mỗi chất 10 gam hòa tan hoàn toàn vào nước thành 200ml dung dịch. Hỏi dung dịch chất nào có nồng độ mol lớn nhất?
Câu hỏi 355 :
Hòa tan 14,28g Na2CO3.10H2O vào 200g nước. Nồng độ % (khối lượng) của dung dịch là:
Câu hỏi 357 :
Trộn 2 lít dung dịch HCl vào 1 lít dung dịch HCl 0,5M. Nồng độ mol của dung dịch mới là:
Câu hỏi 358 :
Cần phải dùng bao nhiêu lít H2SO4 có tỉ khối d = 1,84 và bao nhiêu lít nước cất để pha thành 10 lít dung dịch H2SO4 có d = 1,28?
Câu hỏi 359 :
Rót từ từ nước vào cốc đựng sẵn m gam Na2CO3.10H2O cho đủ 250ml. Khuấy cho muối tan hết, ta được dung dịch Na2CO3 0,1M. Khối lượng của m là:
Câu hỏi 361 :
Cô cạn 150ml dung dịch CuSO4 có khối lượng riêng là 1,2 g/ml thu được 56,25g CuSO4.5H2O. Nồng độ % của dung dịch CuSO4 là:
Cô cạn 150ml dung dịch CuSO4 có khối lượng riêng là 1,2 g/ml thu được 56,25g CuSO4.5H2O. Nồng độ % của dung dịch CuSO4 là:
Câu hỏi 363 :
Tính thể tích dung dịch KOH 5,6% (D = 1,045) cần dùng làm trung hòa hết 350ml dung dịch H2SO4 0,5M.
Tính thể tích dung dịch KOH 5,6% (D = 1,045) cần dùng làm trung hòa hết 350ml dung dịch H2SO4 0,5M.
Câu hỏi 373 :
Những oxit sau: SO2; CO2; CO; CaO; MgO; CaO; Na2O; Al2O3; N2O5; K2O. Những oxit nào vừa tác dụng được với nước, vừa tác dụng được với axit hoặc vừa tác dụng được với nước, vừa tác dụng được với kiềm?
(1): SO2, CO, CO2, CaO, Na2O.
(2): SO2, CO2, N2O5.
(3): Na2O, CaO, Al2O3, MgO, CuO.
(4): Na2O, CaO, K2O.
(5): CuO, Al2O3, MgO, CO, K2O.
Những oxit sau: SO2; CO2; CO; CaO; MgO; CaO; Na2O; Al2O3; N2O5; K2O. Những oxit nào vừa tác dụng được với nước, vừa tác dụng được với axit hoặc vừa tác dụng được với nước, vừa tác dụng được với kiềm?
(1): SO2, CO, CO2, CaO, Na2O.
(2): SO2, CO2, N2O5.
(3): Na2O, CaO, Al2O3, MgO, CuO.
(4): Na2O, CaO, K2O.
(5): CuO, Al2O3, MgO, CO, K2O.
A. (2) (4).
B. (1) (2) (3).
C. (2) (3) (4).
D. (3) (5).
Câu hỏi 374 :
Hợp chất nào sau đây là bazơ?
Hợp chất nào sau đây là bazơ?
A. Đồng (II) nitrat.
B. Kali clorua.
C. Lưu huỳnh đioxit.
D. Canxi hiđroxit.
Câu hỏi 375 :
Một trong những thuốc thử sau có thể dùng để phân biệt dung dịch natri sunfat và dung dịch natri cacbonat.
Một trong những thuốc thử sau có thể dùng để phân biệt dung dịch natri sunfat và dung dịch natri cacbonat.
A. Dung dịch bari clorua.
B. Dung dịch axit clohiđric.
C. Dung dịch chì (II) nitrat.
D. Dung dịch natri hiđroxit.
Câu hỏi 376 :
Ttrong các oxit dưới đây: Al2O3; CaO; CO; Mn2O7; P2O5; N2O5; NO; SiO2; ZnO; Fe2O3.
Oxit axit:
Ttrong các oxit dưới đây: Al2O3; CaO; CO; Mn2O7; P2O5; N2O5; NO; SiO2; ZnO; Fe2O3.
A. Al2O3, CO, P2O5, SiO, NO.
B. P2O5, N2O5, ZnO, Mn2O7.
C. N2O5, P2O5, SiO2, Mn2O7.
D. Al2O3, SiO2, NO.
Câu hỏi 377 :
Ttrong các oxit dưới đây: Al2O3; CaO; CO; Mn2O7; P2O5; N2O5; NO; SiO2; ZnO; Fe2O3.
Oxit bazơ:
Oxit bazơ:
A. Al2O3, CaO, Fe2O3, SiO2.
B. CaO, Fe2O3.
C. Mn2O7, Fe2O3, ZnO, Al2O3.
D. CaO, SiO2, NO, Al2O3, CO.
Câu hỏi 378 :
Ttrong các oxit dưới đây: Al2O3; CaO; CO; Mn2O7; P2O5; N2O5; NO; SiO2; ZnO; Fe2O3.
Oxit lưỡng tính:
Ttrong các oxit dưới đây: Al2O3; CaO; CO; Mn2O7; P2O5; N2O5; NO; SiO2; ZnO; Fe2O3.
Oxit lưỡng tính:
A. Al2O3, ZnO.
B. Mn2O7, SiO2, NO, ZnO.
C. Fe2O3, CO, Al2O3, P2O5.
D. Fe2O3, ZnO, CO, P2O5.
Câu hỏi 379 :
Ttrong các oxit dưới đây: Al2O3; CaO; CO; Mn2O7; P2O5; N2O5; NO; SiO2; ZnO; Fe2O3.
Oxit không tạo muối:
Ttrong các oxit dưới đây: Al2O3; CaO; CO; Mn2O7; P2O5; N2O5; NO; SiO2; ZnO; Fe2O3.
Oxit không tạo muối:
A. CaO, CO, SiO2.
B. CO, NO.
C. NO, ZnO, Mn2O7.
D. CaO, NO, Mn2O7, SiO2.
Câu hỏi 380 :
Để một mẩu natri hiđroxit trên miếng kính trong không khí, sau vài ngày thấy có chất rắn màu trắng phủ ngoài. Nếu nhỏ vài giọt dung dịch HCl vào chất rắn màu trắng thấy có khí không màu, không mùi thoát ra. Chất rắn màu trắng này là sản phẩm của phản ứng natri hiđroxit với:
Để một mẩu natri hiđroxit trên miếng kính trong không khí, sau vài ngày thấy có chất rắn màu trắng phủ ngoài. Nếu nhỏ vài giọt dung dịch HCl vào chất rắn màu trắng thấy có khí không màu, không mùi thoát ra. Chất rắn màu trắng này là sản phẩm của phản ứng natri hiđroxit với:
A. Oxi trong không khí.
B. Hơi nước trong không khí.
C. Cacbon dioxit và oxi trong không khí.
D. Cacbon dioxit trong không khí.
Câu hỏi 381 :
Có ba oxit màu trắng: MgO, Al2O3, Na2O. Có thể nhận biết được các chất đó bằng thuốc thử sau đây không?
Có ba oxit màu trắng: MgO, Al2O3, Na2O. Có thể nhận biết được các chất đó bằng thuốc thử sau đây không?
A. Chỉ dùng nước.
B. Chỉ dùng axit.
C. Chỉ dùng kiềm.
D. Dùng nước và kiềm
Câu hỏi 382 :
Những thí nghiệm nào sau đây sẽ tạo ra chất kết tủa khi trộn:
(1) Dung dịch natri clorua và dung dịch chì nitrat.
(2) Dung dịch natri cacbonat và dung dịch chì kẽm sunfat.
(3) Dung dịch natri sunfat và dung dịch nhôm clorua.
(4) Dung dịch kẽm sunfat và dung dịch đồng (II) clorua.
(5) Dung dịch bari clorua và dung dịch nitrat
Những thí nghiệm nào sau đây sẽ tạo ra chất kết tủa khi trộn:
(1) Dung dịch natri clorua và dung dịch chì nitrat.
(2) Dung dịch natri cacbonat và dung dịch chì kẽm sunfat.
(3) Dung dịch natri sunfat và dung dịch nhôm clorua.
(4) Dung dịch kẽm sunfat và dung dịch đồng (II) clorua.
(5) Dung dịch bari clorua và dung dịch nitrat
A. (1) (2) (5).
B. (1) (2) (3).
C. (2) (4) (5).
D. (3) (4) (5).
Câu hỏi 383 :
(1) H2 + … = Cu + H2O
(2) … + O2 = 2H2O
(3) C + H2O = CO + …
(4) Mg + H2O = … + H2
(5) Mg + 2HCl = … + H2
Các chất được điền vào ô trống lần lượt theo thứ tự
(1) H2 + … = Cu + H2O
(2) … + O2 = 2H2O
(3) C + H2O = CO + …
(4) Mg + H2O = … + H2
(5) Mg + 2HCl = … + H2
Các chất được điền vào ô trống lần lượt theo thứ tự
A. Mg; H2; Cl; O2; H2.
B. CuO; H2; H2; MgO; MgCl2.
C. H2; Cu; Mg; O2; H2O.
D. H2; CuO; MgO; O2; H2.
Câu hỏi 385 :
Có 4 oxit sau:
I. SO3
II. CaO
III. CrO3
IV. MgO
Tập hợp nào sau đây là oxit axit?
Có 4 oxit sau:
I. SO3
II. CaO
III. CrO3
IV. MgO
Tập hợp nào sau đây là oxit axit?
A. I + II.
B. II + III.
C. I + III.
D. III + IV.
Câu hỏi 386 :
Cho phương trình phản ứng sau:
Cho phương trình phản ứng sau:
A. H2SO4, Na2SO4.
B. N2O5, NaNO3.
C. HCl, NaCl.
D. (A) (B) đều đúng.
Câu hỏi 387 :
Có sơ đồ chuyển hóa sau: Biết (X) là chất rắn
Có sơ đồ chuyển hóa sau: Biết (X) là chất rắn
A. X là FeS2; Y là SO3.
B. X là FeS2 hoặc S; Y là SO3.
C. X là O2; Y là SO3.
D. Tất cả đều đúng.
Câu hỏi 388 :
Có năm ống nghiệm chứa các dung dịch sau: Ba(NO3)2, H2SO4, NaOH và Na2CO3. Biết rằng chỉ dùng một hóa chất duy nhất để nhận biết các hóa chất ở trong ống nghiệm.
Có năm ống nghiệm chứa các dung dịch sau: Ba(NO3)2, H2SO4, NaOH và Na2CO3. Biết rằng chỉ dùng một hóa chất duy nhất để nhận biết các hóa chất ở trong ống nghiệm.
A. Dùng phenolphtalein không màu.
B. Dùng giấy quỳ tím.
C. Dùng dung dịch Axit HCl.
D. Dùng dung dịch BaCl2.
Câu hỏi 389 :
Có những chất rắn sau: MgO, P2O5, Ba(OH)2, Na2SO4. Dùng những thuốc thử nào có thể phân biệt được các chất trên?
Có những chất rắn sau: MgO, P2O5, Ba(OH)2, Na2SO4. Dùng những thuốc thử nào có thể phân biệt được các chất trên?
A. Dùng H2O, giấy quỳ tím.
B. Dùng axit H2SO4, phenolphtalein không màu.
C. Dùng dung dịch NaOH, quỳ tím.
D. Tất cả đều sai.
Câu hỏi 390 :
Có năm dung dịch sau đây: Na2CO3, BaCl2, CH3COONa, Ba(HCO3)2 và NaCl. Chỉ dùng dung dịch H2SO4 có thể nhận biết được mấy chất? Số chất biết được là:
Có năm dung dịch sau đây: Na2CO3, BaCl2, CH3COONa, Ba(HCO3)2 và NaCl. Chỉ dùng dung dịch H2SO4 có thể nhận biết được mấy chất? Số chất biết được là:
A. 1.
B. 2.
C. 3.
D. 5.
Câu hỏi 391 :
Để loại bỏ khí CO2 có lẫn trong hỗn hợp (O2, CO2). Người ta cho hỗn hợp đi qua dung dịch chứa:
Để loại bỏ khí CO2 có lẫn trong hỗn hợp (O2, CO2). Người ta cho hỗn hợp đi qua dung dịch chứa:
A. HCl.
B. Na2SO4.
C. NaCl.
D. Ca(OH)2.
Câu hỏi 392 :
Nhỏ một giọt quỳ tím vào dung dịch NaOH, dung dịch có màu xanh, nhỏ từ từ dung dịch HCl cho tới dư vào dung dịch có màu xanh trên thì:
Nhỏ một giọt quỳ tím vào dung dịch NaOH, dung dịch có màu xanh, nhỏ từ từ dung dịch HCl cho tới dư vào dung dịch có màu xanh trên thì:
A. Màu xanh vẫn không thay đổi.
B. Màu xanh nhạt dần rồi mất hẳn.
C. Màu xanh nhạt dần, mất hẳn rồi chuyển sang màu đỏ.
D. Màu xanh đậm thêm dần.
Câu hỏi 393 :
Những cặp chất nào sau đây cùng tồn tại trong một dung dịch?.
Những cặp chất nào sau đây cùng tồn tại trong một dung dịch?.
A. KCl và NaNO3.
B. HCl và AgNO3.
C. KOH và HCl.
D. NaHCO3 và NaOH
Câu hỏi 394 :
Để hòa tan hết 5,1g M2O3 phải dùng 43,8g dung dịch HCl 25%. Công thức của M2O3 là:
Để hòa tan hết 5,1g M2O3 phải dùng 43,8g dung dịch HCl 25%. Công thức của M2O3 là:
A. Fe2O3.
B. Al2O3.
C. Cr2O3.
D. Tất cả đều sai.
Câu hỏi 398 :
Nêu tính chất vật lý, tính chất hóa học của sắt. Về mặt hóa trị sắt có gì khác so với nhôm?
Nêu tính chất vật lý, tính chất hóa học của sắt. Về mặt hóa trị sắt có gì khác so với nhôm?
Câu hỏi 405 :
b. Chỉ được dùng kim loại để phân biệt được các dung dịch sau đây hay không?
NaCl; HCl, NaNO3.
b. Chỉ được dùng kim loại để phân biệt được các dung dịch sau đây hay không?
NaCl; HCl, NaNO3.
Câu hỏi 411 :
Có ba chất là Mg, Al, Al2O3 chỉ được dùng một hóa chất làm thuốc thử phân biệt ba chất trên. Hãy viết phương trình phản ứng.
Có ba chất là Mg, Al, Al2O3 chỉ được dùng một hóa chất làm thuốc thử phân biệt ba chất trên. Hãy viết phương trình phản ứng.
Câu hỏi 413 :
Nêu tính chất của phi kim? Người ta thường căn cứ vào đâu để đánh giá sự mạnh yếu của phi kim?
Nêu tính chất của phi kim? Người ta thường căn cứ vào đâu để đánh giá sự mạnh yếu của phi kim?
Câu hỏi 416 :
Nêu các tính chất lí học và hóa học của clo, viết các phương trình phản ứng minh họa. Tại sao nói clo là phi kim rất mạnh?
Nêu các tính chất lí học và hóa học của clo, viết các phương trình phản ứng minh họa. Tại sao nói clo là phi kim rất mạnh?
Câu hỏi 419 :
Hãy so sánh những tính chất vật lí và tính chất hóa học của CO và CO2. Viết phương trình minh họa.
Hãy so sánh những tính chất vật lí và tính chất hóa học của CO và CO2. Viết phương trình minh họa.
Câu hỏi 420 :
Bằng phương pháp hóa học, hãy làm khô khí ẩm (lẫn hơi nước) của cacbon (II) oxit; cacbon (IV) oxit, hiđro clorua. Giải thích.
Bằng phương pháp hóa học, hãy làm khô khí ẩm (lẫn hơi nước) của cacbon (II) oxit; cacbon (IV) oxit, hiđro clorua. Giải thích.
Câu hỏi 421 :
Vì sao muối cacbonat tác dụng được với nhiều axit và sản phẩm không phải là axit mới? Cho ví dụ minh họa.
Vì sao muối cacbonat tác dụng được với nhiều axit và sản phẩm không phải là axit mới? Cho ví dụ minh họa.
Câu hỏi 429 :
Cân bằng phương trình hóa học và cho biết cacbon trong mỗi trường hợp là chất oxi hóa hay chất khử?
Cân bằng phương trình hóa học và cho biết cacbon trong mỗi trường hợp là chất oxi hóa hay chất khử?
Câu hỏi 430 :
Viết phương trình xảy ra trong các trường hợp sau.
a. Đun nóng Ca(HCO3)2 tác dụng với axit HCl và Ca(OH)2.
Viết phương trình xảy ra trong các trường hợp sau.
a. Đun nóng Ca(HCO3)2 tác dụng với axit HCl và Ca(OH)2.
Câu hỏi 433 :
Dùng bảng tuần hoàn các nguyên tố hóa học, hãy:
a. Đọc tên các nguyên tố trong chu kì 3.
Dùng bảng tuần hoàn các nguyên tố hóa học, hãy:
a. Đọc tên các nguyên tố trong chu kì 3.
Câu hỏi 436 :
Cho nhôm tác dụng với axit HCl.
a. Tính thể tích dung dịch HCl 1,5M cần dùng để tác dụng hết với 8,1g nhôm.
Cho nhôm tác dụng với axit HCl.
a. Tính thể tích dung dịch HCl 1,5M cần dùng để tác dụng hết với 8,1g nhôm.
Câu hỏi 444 :
Cho nhôm tác dụng mạnh với axit HCl.
a. Tính thể tích dung dịch HCl 1,5M cần dùng để tác dụng hết với 8,1g nhôm.
Cho nhôm tác dụng mạnh với axit HCl.
a. Tính thể tích dung dịch HCl 1,5M cần dùng để tác dụng hết với 8,1g nhôm.
Câu hỏi 455 :
Tính thể tích clo thu được ở đktc khi cho 8,7g MnO2 tác dụng với axit HCl đặc, nếu hiệu suất phản ứng là 85%.
Tính thể tích clo thu được ở đktc khi cho 8,7g MnO2 tác dụng với axit HCl đặc, nếu hiệu suất phản ứng là 85%.
Câu hỏi 466 :
Bạn X làm thí nghiệm tìm hiểu về tính hoạt động của các kim loại P, Q, M, N có kết quả như sau:
- Kim loại P đẩy được kim loại Q ra khỏi dung dịch muối.
- Kim loại Q đẩy được hiđro ra khỏi dung dịch axit.
- Kim loại Q đẩy được kim loại M ra khỏi dung dịch muối.
- Kim loại M đẩy được kim loại N ra khỏi dung dịch muối.
Qua kết quả thí nghiệm, bạn X sắp xếp tính hoạt động kim loại như sau:
Bạn X làm thí nghiệm tìm hiểu về tính hoạt động của các kim loại P, Q, M, N có kết quả như sau:
- Kim loại P đẩy được kim loại Q ra khỏi dung dịch muối.
- Kim loại Q đẩy được hiđro ra khỏi dung dịch axit.
- Kim loại Q đẩy được kim loại M ra khỏi dung dịch muối.
- Kim loại M đẩy được kim loại N ra khỏi dung dịch muối.
Qua kết quả thí nghiệm, bạn X sắp xếp tính hoạt động kim loại như sau:
C. P > Q > M < N.
D. P < Q < M < N.
Câu hỏi 467 :
Một bạn học sinh làm thí nghiệm để biết được mức độ hoạt động của kim loại, bằng cách lấy các kim loại M, N, P, Q cho tác dụng riêng biệt ở từng ống nghiệm với cùng thể tích và nồng độ dung dịch HCl có kết quả như sau:
Kim loại
Tác dụng với dung dịch axit HCl
M
Khí hiđro giải phóng ra nhanh.
N
Không quan sát được hiện tượng gì.
P
Khí hiđro giải phóng ra chậm.
Q
Khí hiđro giải phóng ra rất nhanh, dung dịch nóng lên.
Từ kết quả trên, dãy kim loại nào phù hợp với chiều hoạt động của kim loại tăng dần?
Một bạn học sinh làm thí nghiệm để biết được mức độ hoạt động của kim loại, bằng cách lấy các kim loại M, N, P, Q cho tác dụng riêng biệt ở từng ống nghiệm với cùng thể tích và nồng độ dung dịch HCl có kết quả như sau:
|
Kim loại |
Tác dụng với dung dịch axit HCl |
|
M |
Khí hiđro giải phóng ra nhanh. |
|
N |
Không quan sát được hiện tượng gì. |
|
P |
Khí hiđro giải phóng ra chậm. |
|
Q |
Khí hiđro giải phóng ra rất nhanh, dung dịch nóng lên. |
Từ kết quả trên, dãy kim loại nào phù hợp với chiều hoạt động của kim loại tăng dần?
A. Q < P < M < N.
B. M < Q, N < P.
C. Q < M < P < N.
D. N < M < P < Q.
Câu hỏi 468 :
Kim loại M tác dụng với dung dịch HCl sinh ra khí hiđro. Dẫn khí hiđro đi qua oxit của kim loại N nóng, oxit này bị khử cho kim loại N. M và N có thể là:
Kim loại M tác dụng với dung dịch HCl sinh ra khí hiđro. Dẫn khí hiđro đi qua oxit của kim loại N nóng, oxit này bị khử cho kim loại N. M và N có thể là:
A. Đồng và Chì (Cu và Pb).
B. Chì và Kẽm (Pb và Zn).
C. Kẽm và Đồng (Zn và Cu).
D. Đồng và Bạc (Cu và Ag).
Câu hỏi 469 :
Ngâm một lá sắt sạch trong dung dịch đồng (II) sunfat.
Câu trả lời nào sau đây là đúng nhất?
Ngâm một lá sắt sạch trong dung dịch đồng (II) sunfat.
Câu trả lời nào sau đây là đúng nhất?
B. Đồng được giải phóng, nhưng sắt không biến đổi.
C. Sắt bị hòa tan một phần và đồng được giải phóng.
D. Không có chất nào mới được sinh ra, chỉ có sắt bị hòa tan.
Câu hỏi 470 :
Có những kim loại sau:
Hãy chọn một kim loại:
a. Phản ứng mạnh với dung dịch axit clohiđric.
Có những kim loại sau:
Hãy chọn một kim loại:
a. Phản ứng mạnh với dung dịch axit clohiđric.
A. Đồng (Cu).
B. Phatin (Pt).
C. Nhôm (Al).
D. Kẽm (Zn).
Câu hỏi 471 :
b. Không tác dụng với oxi thậm chí kim loại nóng đỏ.
b. Không tác dụng với oxi thậm chí kim loại nóng đỏ.
A. Đồng (Cu).
B. Phatin (Pt).
C. Nhôm (Al).
D. Kẽm (Zn).
Câu hỏi 472 :
c. Nhẹ, dẫn điện và dẫn nhiệt tốt.
c. Nhẹ, dẫn điện và dẫn nhiệt tốt.
A. Đồng (Cu).
B. Phatin (Pt).
C. Nhôm (Al).
D. Kẽm (Zn).
Câu hỏi 473 :
d. Trở thành màu đen khi đốt trong không khí.
d. Trở thành màu đen khi đốt trong không khí.
A. Đồng (Cu).
B. Phatin (Pt).
C. Nhôm (Al).
D. Kẽm (Zn).
Câu hỏi 474 :
Cho các kim loại K; Ca; Al lần lượt tác dụng với dung dịch HCl. Nếu cho cùng số mol, mỗi kim loại trên tác dụng với axit HCl thì kim loại nào cho nhiều hiđro hơn?
Cho các kim loại K; Ca; Al lần lượt tác dụng với dung dịch HCl. Nếu cho cùng số mol, mỗi kim loại trên tác dụng với axit HCl thì kim loại nào cho nhiều hiđro hơn?
A. Al.
B. K.
C. K và Ca.
D. Ca.
Câu hỏi 475 :
Cho 65g kim loại kẽm tác dụng với axit clohiđric cho 136g ZnCl2 và giải phóng 22,4 lít khí hiđro (đktc). Khối lượng axit HCl cần dùng là:
Cho 65g kim loại kẽm tác dụng với axit clohiđric cho 136g ZnCl2 và giải phóng 22,4 lít khí hiđro (đktc). Khối lượng axit HCl cần dùng là:
A. 73g.
B. 72g.
C. 36,5g.
D. 71g.
Câu hỏi 476 :
Trong phòng thí nghiệm người ta điều chế khí hiđro bằng cách cho Zn tác dụng với axit clohiđric HCl theo sơ đồ sau:
Kẽm + axit clohiđric kẽm clorua + khí hiđro.
Nếu cho 13g Zn tác dụng hết với dung dịch HCl 0,4M thì thể tích khí hiđro thu được là bao nhiêu?
Trong phòng thí nghiệm người ta điều chế khí hiđro bằng cách cho Zn tác dụng với axit clohiđric HCl theo sơ đồ sau:
Kẽm + axit clohiđric kẽm clorua + khí hiđro.
Nếu cho 13g Zn tác dụng hết với dung dịch HCl 0,4M thì thể tích khí hiđro thu được là bao nhiêu?
A. 3 lít.
B. 3,3 lít.
C. 3,36 lít.
D. 5,36 lít.
Câu hỏi 477 :
Cho 8,4g bột sắt cháy hết trong 2,24 lít khí oxi tạo ra oxit sắt từ (Fe3O4). Khối lượng oxit sắt tạo thành là:
Cho 8,4g bột sắt cháy hết trong 2,24 lít khí oxi tạo ra oxit sắt từ (Fe3O4). Khối lượng oxit sắt tạo thành là:
A. 11,4g.
B. 11,6g.
C. 12g.
D. 20g.
Câu hỏi 478 :
Tính chất nào sau đây không phải là của khí clo?
Tính chất nào sau đây không phải là của khí clo?
A. Tan hoàn toàn trong nước.
B. Có màu vàng lục.
C. Có tính tẩy trắng khi ẩm.
D. Mùi hắc, rất độc.
Câu hỏi 479 :
Biết nhiều phi kim tác dụng được với oxi để tạo oxit phi kim tương ứng. Vậy dãy phi nào dưới đây tác dụng được với oxi?
Biết nhiều phi kim tác dụng được với oxi để tạo oxit phi kim tương ứng. Vậy dãy phi nào dưới đây tác dụng được với oxi?
A. C, S, P, Si.
B. Cl2, Br2, C, N2.
C. I, F, Ne, Si.
D. He, P, S, Br2.
Câu hỏi 480 :
Cho các hỗn hợp khí sau:
1. H2 và O2. 2. SO2 và O2. 3. H2 và Cl2
tồn tại trong những điều kiện nào?
Cho các hỗn hợp khí sau:
1. H2 và O2. 2. SO2 và O2. 3. H2 và Cl2
tồn tại trong những điều kiện nào?
A. Tồn tại bất cứ điều kiện nào.
B. Tồn tại ở nhiệt độ thấp không có xúc tác (hoặc trong bóng tối).
C. Không thể tồn tại vì có phản ứng xảy ra.
D. Tất cả đều sai.
Câu hỏi 481 :
Dãy những phi kim nào dưới đây không tác dụng được với nhau?
Dãy những phi kim nào dưới đây không tác dụng được với nhau?
A. N2, H2, S, O2, C.
B. P, H2, S, Cl2, I2.
C. O2, Cl2, I2, Si.
D. B, Br2, I2, P.
Câu hỏi 482 :
Một trong những quá trình nào sau đây không sinh ra khí cacbonix?
Một trong những quá trình nào sau đây không sinh ra khí cacbonix?
A. Đốt cháy khí đốt tự nhiên.
B. Sản xuất gang thép.
C. Sản xuất vôi sống.
D. Quang hợp của cây xanh.
Câu hỏi 483 :
Tính chất vật lí nào sau đây là của cacbon oxit (CO)?
A. Khí cháy, không độc, không màu.
B. Khí cháy, độc, không màu.
C. Khí không cháy, không màu, rất nhẹ (bằng 1/7 khối lượng của không khí).
D. Khí màu lục nhạt, độc, nặng hơn không khí (gấp 2,5 lần không khí).
Câu hỏi 484 :
Bằng phương pháp hóa học làm thế nào để nhận ra sự có mặt của mỗi khí trong hỗn hợp gồm: CO, CO2, SO3?
Bằng phương pháp hóa học làm thế nào để nhận ra sự có mặt của mỗi khí trong hỗn hợp gồm: CO, CO2, SO3?
A. Dẫn hỗn hợp qua dung dịch BaCl2.
B. Dẫn hỗn hợp qua dung dịch Ca(OH)2.
C. Dẫn hỗn hợp qua dung dịch BaCl2, sau đó qua nước vôi trong dư,
D. Tất cả đều sai.
Câu hỏi 485 :
Có những khí ẩm (khí có lẫn hơi nước) sau đây:
a. Amoniac.
b. Sunfurơ.
c. Cacbon dioxit.
d. Hiđro clorua.
1. Khí ẩm nào có thể làm khô bằng axit sunfuric đặc?
Có những khí ẩm (khí có lẫn hơi nước) sau đây:
a. Amoniac.
b. Sunfurơ.
c. Cacbon dioxit.
d. Hiđro clorua.
1. Khí ẩm nào có thể làm khô bằng axit sunfuric đặc?
A. b, c, a.
B. a, b, c.
C. b, c, d.
D. c, d, a.
Câu hỏi 486 :
2. Khí ẩm nào có thể làm khô bằng canxi oxit?
2. Khí ẩm nào có thể làm khô bằng canxi oxit?
A. a.
B. a, d, b.
C. b, c, d.
D. c, d, a.
Câu hỏi 488 :
Nguyên tố X tạo được hợp chất sau: XH3 và X2H5. Trong bảng hệ thống tuần hoàn các nguyên tố hóa học, nguyên tố X cùng nhóm với:
Nguyên tố X tạo được hợp chất sau: XH3 và X2H5. Trong bảng hệ thống tuần hoàn các nguyên tố hóa học, nguyên tố X cùng nhóm với:
A. Agan.
B. Nitơ.
C. Oxi.
D. Flo.
Câu hỏi 489 :
Đốt cháy 10cm3 khí hiđro trong 10cm3 khí oxi. Thể tích chất khí còn lại sau phản ứng:
Đốt cháy 10cm3 khí hiđro trong 10cm3 khí oxi. Thể tích chất khí còn lại sau phản ứng:
A. 5 cm3 hiđro.
B. 10 cm3 hiđro.
C. Chỉ có 10 cm3 hơi nước.
D. 5 cm3 oxi.
Câu hỏi 490 :
Khi cho 13g kẽm tác dụng với 0,3 mol HCl. Khối lượng muối ZnCl2 được tạo thành trong phản ứng này là:
Khi cho 13g kẽm tác dụng với 0,3 mol HCl. Khối lượng muối ZnCl2 được tạo thành trong phản ứng này là:
A. 20,4g.
B. 10,2g.
C. 30,6g.
D. 40g.
Câu hỏi 491 :
Cho 1,35g nhôm tác dụng với dung dịch chứa 7,3g HCl. Khối lượng muối tạo thành là:
Cho 1,35g nhôm tác dụng với dung dịch chứa 7,3g HCl. Khối lượng muối tạo thành là:
A. 3,3375g.
B. 6,755g.
C. 7,775g.
D. 10,775g.
Câu hỏi 492 :
Cho 8,125g Zn tác dụng với dung dịch loãng có chứa 18,25g axit clohiđric HCl. Thể tích khí H2 (ở đktc) sinh ra là:
Cho 8,125g Zn tác dụng với dung dịch loãng có chứa 18,25g axit clohiđric HCl. Thể tích khí H2 (ở đktc) sinh ra là:
A. 2,8 lít.
B. 2,75 lít.
C. 2,81 lít.
D. 3,85 lít.
Câu hỏi 493 :
Trộn 50ml dung dịch Ba(OH)2 0,04M với 150ml dung dịch HCl 0,06M thu được 200ml dung dịch N. Nồng độ mol/l của muối BaCl2 trong dung dịch B bằng:
Trộn 50ml dung dịch Ba(OH)2 0,04M với 150ml dung dịch HCl 0,06M thu được 200ml dung dịch N. Nồng độ mol/l của muối BaCl2 trong dung dịch B bằng:
A. 0,05M.
B. 0,01M.
C. 0,17M.
D. 0,08M.
Câu hỏi 494 :
Hòa tan hoàn toàn 2,84g hỗn hợp 2 muối cacbonat của 2 kim loại có hóa trị II thuộc chu kỳ khác nhau trong hệ thống tuần hoàn bằng dung dịch axit HCl ta thu được 0,672ml khí CO2 (đo ở đktc). Biết kim loại này có số mol gấp đôi kim loại kia. Kim loại đó là:
Hòa tan hoàn toàn 2,84g hỗn hợp 2 muối cacbonat của 2 kim loại có hóa trị II thuộc chu kỳ khác nhau trong hệ thống tuần hoàn bằng dung dịch axit HCl ta thu được 0,672ml khí CO2 (đo ở đktc). Biết kim loại này có số mol gấp đôi kim loại kia. Kim loại đó là:
A. Ba và Ag.
B. Ca và Cu.
C. Fe và Zn.
D. Mg và Ca,
Câu hỏi 495 :
Nêu phương pháp hóa học để có thể phân biệt các chất trong mỗi nhóm chất sau:
a. Etilen và metan.
Nêu phương pháp hóa học để có thể phân biệt các chất trong mỗi nhóm chất sau:
a. Etilen và metan.
Câu hỏi 496 :
Nêu phương pháp hóa học để có thể phân biệt các chất trong mỗi nhóm chất sau:
b. Etilen, hiđro và khí cacbonic.
Nêu phương pháp hóa học để có thể phân biệt các chất trong mỗi nhóm chất sau:
b. Etilen, hiđro và khí cacbonic.
Câu hỏi 497 :
Nêu phương pháp hóa học để có thể phân biệt các chất trong mỗi nhóm chất sau:
c. Etilen, metan và hiđro.
Nêu phương pháp hóa học để có thể phân biệt các chất trong mỗi nhóm chất sau:
c. Etilen, metan và hiđro.
Câu hỏi 498 :
a. Viết công thức cấu tạo của metan. Các liên kết trong phân tử metan gọi là liên kết gì?
a. Viết công thức cấu tạo của metan. Các liên kết trong phân tử metan gọi là liên kết gì?
Câu hỏi 499 :
b. Cho clo và metan vào một ống nghiệm. Làm thế nào để phản ứng có thể xảy ra. Làm thế nào để biết các phản ứng đã xảy ra?
b. Cho clo và metan vào một ống nghiệm. Làm thế nào để phản ứng có thể xảy ra. Làm thế nào để biết các phản ứng đã xảy ra?
Câu hỏi 502 :
Nêu phương pháp hóa học để phân biệt các khí sau: cacbon (II) oxit; khí cacbonic; metan.
Nêu phương pháp hóa học để phân biệt các khí sau: cacbon (II) oxit; khí cacbonic; metan.
Câu hỏi 504 :
Cho benzen tác dụng với hiđro khi đun nóng, có mặt Ni xúc tác. Viết phương trình phản ứng dưới dạng công thức cấu tạo.
Cho benzen tác dụng với hiđro khi đun nóng, có mặt Ni xúc tác. Viết phương trình phản ứng dưới dạng công thức cấu tạo.
Câu hỏi 506 :
Trình bày phương pháp hóa học để thu được khí CH4 tinh khiết từ hỗn hợp khí gồm CH4 và C2H4. Viết phản ứng xảy ra.
Trình bày phương pháp hóa học để thu được khí CH4 tinh khiết từ hỗn hợp khí gồm CH4 và C2H4. Viết phản ứng xảy ra.
Câu hỏi 507 :
Viết phản ứng đốt cháy metan và benzen. Có hiện tượng gì khác nhau trong hai phản ứng đốt cháy?
Viết phản ứng đốt cháy metan và benzen. Có hiện tượng gì khác nhau trong hai phản ứng đốt cháy?
Câu hỏi 509 :
Có thể dùng nước brom để phân biệt 3 chất khí CH4, C2H4, C2H2 được không? Nếu được hãy nói rõ cách làm.
Có thể dùng nước brom để phân biệt 3 chất khí CH4, C2H4, C2H2 được không? Nếu được hãy nói rõ cách làm.
Câu hỏi 512 :
Cho biết những phương pháp chủ yếu để chế biến dầu mỏ. Nêu một số sản phẩm chính khi chưng cất dầu mỏ.
Cho biết những phương pháp chủ yếu để chế biến dầu mỏ. Nêu một số sản phẩm chính khi chưng cất dầu mỏ.
Câu hỏi 514 :
b. Khi ngọn đèn dầu có bấc ngắn lụi dần, vì dầu đã cạn, người ta đổ nước vào dầu còn lại thì đèn lại sáng lên.
b. Khi ngọn đèn dầu có bấc ngắn lụi dần, vì dầu đã cạn, người ta đổ nước vào dầu còn lại thì đèn lại sáng lên.
Câu hỏi 523 :
Viết phương trình phản ứng xảy ra khi cho axit axetic tác dụng lần lượt với kali hiđroxit, vôi tôi, bột magie và đá vôi.
Viết phương trình phản ứng xảy ra khi cho axit axetic tác dụng lần lượt với kali hiđroxit, vôi tôi, bột magie và đá vôi.
Câu hỏi 524 :
Cho 2 chất lỏng là axit axetic và rượu etylic. Trình bày hai phương pháp phân biệt chúng bằng phản ứng hóa học.
Cho 2 chất lỏng là axit axetic và rượu etylic. Trình bày hai phương pháp phân biệt chúng bằng phản ứng hóa học.
Câu hỏi 527 :
Điền công thức hóa chất thích hợp vào chỗ có dấu … và cân bằng các phương trình phản ứng.
Câu hỏi 529 :
Trình bày phương pháp hóa học để phân biệt ba chất lỏng sau: benzen, rượu etylic và axit axetic.
Trình bày phương pháp hóa học để phân biệt ba chất lỏng sau: benzen, rượu etylic và axit axetic.
Câu hỏi 530 :
Hãy kể tên một loại chất béo có nguồn gốc động vật và một loại chất béo có nguồn gốc thực vật.
Câu hỏi 531 :
Có gì khác nhau căn bản giữa dầu lạc và dầu bôi trơn máy móc về thành phần cấu tạo và tính chất hóa học?
Có gì khác nhau căn bản giữa dầu lạc và dầu bôi trơn máy móc về thành phần cấu tạo và tính chất hóa học?
Câu hỏi 535 :
a. Trình bày phương pháp hóa học để phân biệt bốn dung dịch không màu sau: rượu etylic, axit axetic, glucozơ và saccarozơ.
a. Trình bày phương pháp hóa học để phân biệt bốn dung dịch không màu sau: rượu etylic, axit axetic, glucozơ và saccarozơ.
Câu hỏi 545 :
b. Làm lạnh khí sản phẩm tới nhiệt độ phòng thì thu được bao nhiêu ml chất lỏng (d = 0,879 g/ml)
b. Làm lạnh khí sản phẩm tới nhiệt độ phòng thì thu được bao nhiêu ml chất lỏng (d = 0,879 g/ml)
Câu hỏi 562 :
Cho 60g CH3COOH tác dụng 100g CH3CH2OH thu được 55g CH3COOCH2CH3. Tính hiệu suất phản ứng.
Cho 60g CH3COOH tác dụng 100g CH3CH2OH thu được 55g CH3COOCH2CH3. Tính hiệu suất phản ứng.
Câu hỏi 564 :
b. Cần bao nhiêu ml dung dịch X để trung hòa 25ml dung dịch, hỗn hợp Ba(OH)2 0,2M và NaOH 0,05M.
b. Cần bao nhiêu ml dung dịch X để trung hòa 25ml dung dịch, hỗn hợp Ba(OH)2 0,2M và NaOH 0,05M.
Câu hỏi 565 :
Những chất nào sau đây đều là hidrocacbon?
Những chất nào sau đây đều là hidrocacbon?
A. FeCl; C2H6O; CH4; NaHCO3.
B. NaC6H5; CH4O; HNO3; C6H6.
C. CH4; C2H4; C2H2; C6H6.
D. CH3NO2; CH3Br; NaOH.
Câu hỏi 566 :
Một trong những phương pháp nào sau đây là tốt nhất để phân biệt khí metan và khí etilen?
Một trong những phương pháp nào sau đây là tốt nhất để phân biệt khí metan và khí etilen?
A. Dựa vào tỉ lệ về thể tích khí oxi tham gia phản ứng đốt chát.
B. Sự thay đổi màu dung dịch nước brom.
C. So sánh khối lượng riêng (g/l).
D. Phân tích thành phần định lượng của các hợp chất.
Câu hỏi 567 :
Những chất nào sau đây khi tham gia phản ứng có phản ứng cộng và phản ứng thế?
A. Metan.
B. Benzen.
C. Axetilen.
D. Etilen.
Câu hỏi 568 :
Những hidrocacbon nào sau đây trongphat vừa có liên kết đơn, vừa có liên kết đôi?
Những hidrocacbon nào sau đây trongphat vừa có liên kết đơn, vừa có liên kết đôi?
A. Etilen.
B. Benzen.
C. Metan.
D. Axetilen.
Câu hỏi 569 :
Những hidrocacbon nào sau đây trong phân tử vừa có liên kết đơn, vừa có liên kết ba?
Những hidrocacbon nào sau đây trong phân tử vừa có liên kết đơn, vừa có liên kết ba?
A. Etilen.
B. Benzen.
C. Metan.
D. Axetilen
Câu hỏi 570 :
Khí đốt nhiên liệu hidrocacbon, một trong những sản phẩm chính là khí A. Khí A tác dụng với hơi nước trong không khí tạo ra axit yếu. Tên của khí A là gì?
Khí đốt nhiên liệu hidrocacbon, một trong những sản phẩm chính là khí A. Khí A tác dụng với hơi nước trong không khí tạo ra axit yếu. Tên của khí A là gì?
A. SO2.
B. CO2.
C. NH3.
D. CO.
Câu hỏi 571 :
Có 5 dung dịch sau đây: Na2CO3, BaCl2, CH3COOK, Ba(HCO3)2 và NaCl. Chỉ dùng dung dịch H2SO4 có thể nhận biết được mấy chất?
Có 5 dung dịch sau đây: Na2CO3, BaCl2, CH3COOK, Ba(HCO3)2 và NaCl. Chỉ dùng dung dịch H2SO4 có thể nhận biết được mấy chất?
A. 5.
B. 2.
C. 3.
D. 4.
Câu hỏi 572 :
Để tẩy sạch vết dầu mỡ hoặc chất béo dính vào quần áo. Ta có thể dùng chất nào sau đây:
Để tẩy sạch vết dầu mỡ hoặc chất béo dính vào quần áo. Ta có thể dùng chất nào sau đây:
B. Dầu hỏa.
C. Dung dịch nước clo.
D. Rượu etylic.
Câu hỏi 573 :
Một trong những chất nào sau đây không tác dụng với natri, giải phóng hiđro.
Một trong những chất nào sau đây không tác dụng với natri, giải phóng hiđro.
A. H2O.
B. Axit axetic.
C. Dầu hỏa.
D. Rượu etylic.
Câu hỏi 574 :
Một trong những chất nào sau đây không tác dụng với natri giải phóng khí hiđro?
Một trong những chất nào sau đây không tác dụng với natri giải phóng khí hiđro?
A. Nước.
B. Axit axetic.
C. Rượu etylic.
D. Dầu hỏa.
Câu hỏi 575 :
Các loại thực phẩm nào là hợp chất cao phân tử (polime)?
Các loại thực phẩm nào là hợp chất cao phân tử (polime)?
A. Gluxit và chất béo.
B. Protit và Gluxit.
C. Protit và chất béo.
D. Gluxit, chất béo và Protit.
Câu hỏi 576 :
Các chất nào sau đây được sản xuất từ nguyên liệu là xenlulozơ?
Các chất nào sau đây được sản xuất từ nguyên liệu là xenlulozơ?
A. Tơ nhân tạo.
B. Rượu etylic.
C. Boxit.
D. Glucozơ.
Câu hỏi 577 :
Xác định chất có trong sơ đồ sau:
X, Y, M là những chất nào trong các dãy chất sau?
Xác định chất có trong sơ đồ sau:
X, Y, M là những chất nào trong các dãy chất sau?
A. CH4, CO2, CH3COOH.
B. C2H4, C2H5OH, H2O.
C. C2H5OH, CO2, CH3COOH.
D. A, B đều đúng.
Câu hỏi 578 :
Từ các chất CH3COOH, C2H5OH, CH4, CH3COONa. Hãy lập mối quan hệ của các chất theo sơ đồ sau:
Có mấy chuỗi biến hóa theo sơ đồ trên?
Từ các chất CH3COOH, C2H5OH, CH4, CH3COONa. Hãy lập mối quan hệ của các chất theo sơ đồ sau:
Có mấy chuỗi biến hóa theo sơ đồ trên?
A. 1.
B. 2.
C. 3.
D. 4.
Câu hỏi 579 :
Từ các chất vô cơ nào sau đây điều chế được P.V.C, P.E và C6H12.
A. Na2CO3, S.
B. CaCO3, C.
C. K2CO3, P.
D. Tất cả đều được.
Câu hỏi 580 :
Ba gói bột màu trắng là glucozơ, tinh bột và saccarozơ, có thể phân biệt bằng cách sau đây không?
Ba gói bột màu trắng là glucozơ, tinh bột và saccarozơ, có thể phân biệt bằng cách sau đây không?
A. Hòa tan vào nước, và cho phản ứng với AgNO3/NH3.
B. Dùng dung dịch Iot và Cu(OH)2.
C. Dùng dung dịch nước vôi đặc (CaO.H2O) và dung dịch Iot.
D. Tất cả đều đúng.
Câu hỏi 581 :
Các yếu tố nào sau đây làm ảnh hưởng phản ứng xảy ra theo chiều thuận (chiều tạo sản phẩm) giữa axit axetic và rượu etylic?
1. Nhiệt độ.
2. Chất xúc tác.
3. Nồng độ của các chất phản ứng.
4. Bản chất các chất phản ứng.
Các yếu tố nào sau đây làm ảnh hưởng phản ứng xảy ra theo chiều thuận (chiều tạo sản phẩm) giữa axit axetic và rượu etylic?
1. Nhiệt độ.
2. Chất xúc tác.
3. Nồng độ của các chất phản ứng.
4. Bản chất các chất phản ứng.
A. 1, 3.
B. 2, 4.
C. 1, 2, 3.
D. 1, 2, 3, 4.
Câu hỏi 582 :
Có ba lọ chứa các dung dịch sau: rượu etylic, glucozơ và axit axetic. Có thể dùng các thuốc thử nào sau đây để phân biệt.
Có ba lọ chứa các dung dịch sau: rượu etylic, glucozơ và axit axetic. Có thể dùng các thuốc thử nào sau đây để phân biệt.
A. Giấy quỳ tím và Na.
B. Na và AgNO3/NH3.
C. Giấy quỳ tím và AgNO3/NH3.
D. Tất cả đều đúng.
Câu hỏi 583 :
Có thể phân biệt được các chất sau: Lòng trắng trứng, glucozơ và đường saccarozơ bằng 1 thuốc thử duy nhất sau không?
Có thể phân biệt được các chất sau: Lòng trắng trứng, glucozơ và đường saccarozơ bằng 1 thuốc thử duy nhất sau không?
A. Na.
B. Cu(OH)2.
C. HNO3.
D. Dung dịch Iot.
Câu hỏi 584 :
Có 2 chất lỏng axit axetic và rượu etylic. Có mấy cách phân biệt các chất đó?
Có 2 chất lỏng axit axetic và rượu etylic. Có mấy cách phân biệt các chất đó?
A. 1.
B. 2.
C. 3.
D. 4.
Câu hỏi 585 :
Phân tích 5g chất hữu cơ, cho sản phẩm qua bình đựng đá bọt tẩm H2SO4 đặc, bình nặng thêm 5,4g. Thành phần % khối lượng của hiđro là:
Phân tích 5g chất hữu cơ, cho sản phẩm qua bình đựng đá bọt tẩm H2SO4 đặc, bình nặng thêm 5,4g. Thành phần % khối lượng của hiđro là:
A. 3%.
B. 8%.
C. 10%.
D. 12%.
Câu hỏi 586 :
Đốt chát 1,6g chất hữu cơ gồm 2 nguyên tố là A và hiđro, thu được 3,6g nước. Thành phần % khối lượng của A là:
Đốt chát 1,6g chất hữu cơ gồm 2 nguyên tố là A và hiđro, thu được 3,6g nước. Thành phần % khối lượng của A là:
A. 50%.
B. 75%.
C. 80%.
D. Không xác định được.
Câu hỏi 587 :
Khi đốt cháy hoàn toàn hidrocacbon X thu được tỉ lệ số mol CO2 và hơi nước bằng 2 : 1. Vậy X là:
Khi đốt cháy hoàn toàn hidrocacbon X thu được tỉ lệ số mol CO2 và hơi nước bằng 2 : 1. Vậy X là:
A. C2H4.
B. C6H12.
C. C3H8.
D. C2H2.
Câu hỏi 588 :
Trộn hai thể tích khí CH4 và 1 thể tích khí C2H4 thu được ở 6,72 lít hỗn hợp khí (đo ở đktc). Đốt cháy hết hỗn hợp khí trên, thể tích khí CO2 thu được ở đktc là:
Trộn hai thể tích khí CH4 và 1 thể tích khí C2H4 thu được ở 6,72 lít hỗn hợp khí (đo ở đktc). Đốt cháy hết hỗn hợp khí trên, thể tích khí CO2 thu được ở đktc là:
A. 6,72 lít.
B. 8,96 lít.
C. 9 lít.
D. 10,5 lít.
Câu hỏi 589 :
Hỗn hợp khí A (đktc) chứa những thể tích như nhau CH4 và C3H8. Vậy 1 lít hỗn hợp A nặng:
Hỗn hợp khí A (đktc) chứa những thể tích như nhau CH4 và C3H8. Vậy 1 lít hỗn hợp A nặng:
A. 0,72kg.
B. 1,20g.
C. 1,34g.
D. Các giá trị cho trên đều không phù hợp.
Câu hỏi 590 :
Đốt cháy một hidrocacbon X ta thu được số mol CO2 và H2O theo tỉ lệ 2 : 1. X là một chất không có đồng phân. Vậy X có công thức phân tử là:
Đốt cháy một hidrocacbon X ta thu được số mol CO2 và H2O theo tỉ lệ 2 : 1. X là một chất không có đồng phân. Vậy X có công thức phân tử là:
A. C2H2.
B. C6H6.
C. C4H4.
D. C4H8.
Câu hỏi 591 :
Khi hòa tan 50g đường glucozơ (C6H12O6) vào 250g nước ở 20oC thì thu được dung dịch bão hòa. Độ tan của đường ở 20oC là:
Khi hòa tan 50g đường glucozơ (C6H12O6) vào 250g nước ở 20oC thì thu được dung dịch bão hòa. Độ tan của đường ở 20oC là:
A. 20g.
B. 10g.
C. 15g.
D. 30g.
Câu hỏi 597 :
Đốt cháy 0,64g lưu huỳnh ta được chất A. Hòa tan chất A vào 200g H2O thì thu được dung dịch B. Tính C% của dung dịch B.
Đốt cháy 0,64g lưu huỳnh ta được chất A. Hòa tan chất A vào 200g H2O thì thu được dung dịch B. Tính C% của dung dịch B.
Câu hỏi 599 :
b. Biết hai oxit có tỉ lệ số mol là 1 : 1.
Tính khối lượng của mỗi oxit và mỗi bazơ trong hỗn hợp đầu.
b. Biết hai oxit có tỉ lệ số mol là 1 : 1.
Tính khối lượng của mỗi oxit và mỗi bazơ trong hỗn hợp đầu.
Câu hỏi 600 :
Trung hòa 400ml dung dịch H2SO4 2M bằng dung dịch NaOH 20%.
a. Viết phương trình phản ứng xảy ra.
Trung hòa 400ml dung dịch H2SO4 2M bằng dung dịch NaOH 20%.
a. Viết phương trình phản ứng xảy ra.
Câu hỏi 602 :
Hòa tan hết 128g hỗn hợp Mg và MgO phải dùng 400ml dung dịch HCl 2M.
a. Tính % khối lượng chất ban đầu.
Hòa tan hết 128g hỗn hợp Mg và MgO phải dùng 400ml dung dịch HCl 2M.
a. Tính % khối lượng chất ban đầu.
Câu hỏi 604 :
b. Cho một lượng NaOH dư vào dung dịch sau phản ứng sẽ thu được bao nhiêu gam kết tủa?
b. Cho một lượng NaOH dư vào dung dịch sau phản ứng sẽ thu được bao nhiêu gam kết tủa?
Câu hỏi 609 :
Hòa tan một lượng sắt vào 500ml dung dịch H2SO4 (vừa đủ) thu được 33,6 lít khí hiđro (đktc).
a. Tính khối lượng sắt đã dùng.
Hòa tan một lượng sắt vào 500ml dung dịch H2SO4 (vừa đủ) thu được 33,6 lít khí hiđro (đktc).
a. Tính khối lượng sắt đã dùng.
Câu hỏi 632 :
Cần phải lấy bao nhiêu gam Na2CO3.10H2O và bao nhiêu gam nước để pha chế được 1000g dung dịch Na2CO3 5,3%?
Cần phải lấy bao nhiêu gam Na2CO3.10H2O và bao nhiêu gam nước để pha chế được 1000g dung dịch Na2CO3 5,3%?
Câu hỏi 636 :
Đốt 5,6 lít etilen. Hãy tính thể tích không khí cần dùng, biết rằng oxi chiếm 20% thể tích không khí (đktc).
Đốt 5,6 lít etilen. Hãy tính thể tích không khí cần dùng, biết rằng oxi chiếm 20% thể tích không khí (đktc).
Câu hỏi 637 :
Cho nhôm cacbua tác dụng với nước thì được khí metan và nhôm hiđroxit.
a. Tính lượng nhôm cacbua cần dùng để có 4,8g metan.
Cho nhôm cacbua tác dụng với nước thì được khí metan và nhôm hiđroxit.
a. Tính lượng nhôm cacbua cần dùng để có 4,8g metan.
Câu hỏi 638 :
b. Để dung hòa bazơ tạo thành sau phản ứng, phải dùng một khối lượng dung dịch axit clohiđric 10% là bao nhiêu?
b. Để dung hòa bazơ tạo thành sau phản ứng, phải dùng một khối lượng dung dịch axit clohiđric 10% là bao nhiêu?
Câu hỏi 641 :
Đốt cháy một hỗn hợp 25cm3 metan và etylen cần 60cm3 oxi.
a. Tính thể tích mỗi chất khí.
Đốt cháy một hỗn hợp 25cm3 metan và etylen cần 60cm3 oxi.
a. Tính thể tích mỗi chất khí.
Câu hỏi 647 :
Hỗn hợp khí X gồm CH4 và CxHy có tỉ lệ thể tích 1 : 1. Biết 1 lít hỗn hợp khí X (ở đktc) nặng 0,9275g. Vậy công thức phân tử của CxHy là:
Hỗn hợp khí X gồm CH4 và CxHy có tỉ lệ thể tích 1 : 1. Biết 1 lít hỗn hợp khí X (ở đktc) nặng 0,9275g. Vậy công thức phân tử của CxHy là:
A. C2H6.
B. C2H2.
C. C3H8.
D. C4H8.
Câu hỏi 649 :
b. Tính lượng xà phòng bánh thu được, nếu phản ứng xảy ra hoàn toàn và trong xà phòng có chứa 60% khối lượng C17H35COONa?
b. Tính lượng xà phòng bánh thu được, nếu phản ứng xảy ra hoàn toàn và trong xà phòng có chứa 60% khối lượng C17H35COONa?
Câu hỏi 651 :
Cho 60g CH3COOH tác dụng với 100g C2H5OH ta thu được 55g este là etyl axetat. Tính hiệu quất phản ứng xảy ra.
Cho 60g CH3COOH tác dụng với 100g C2H5OH ta thu được 55g este là etyl axetat. Tính hiệu quất phản ứng xảy ra.
Lời giải có ở chi tiết câu hỏi nhé! (click chuột vào câu hỏi).
Copyright © 2021 HOCTAPSGK