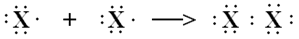Hoá học 10 Bài 21 Khái quát về nhóm halogen
Tóm tắt bài
1.1. Vị trí của nhóm halogen trong Bảng tuần hoàn
- Nhóm halogen gồm : Flo(F); Clo(Cl); Brom (Br), Iot (I), Atatin (At)
- Các nguyên tố halogen thuộc nhóm VIIA. Chúng đứng gần cuối các chu kì, ngay trước các nguyên tố khí hiếm.
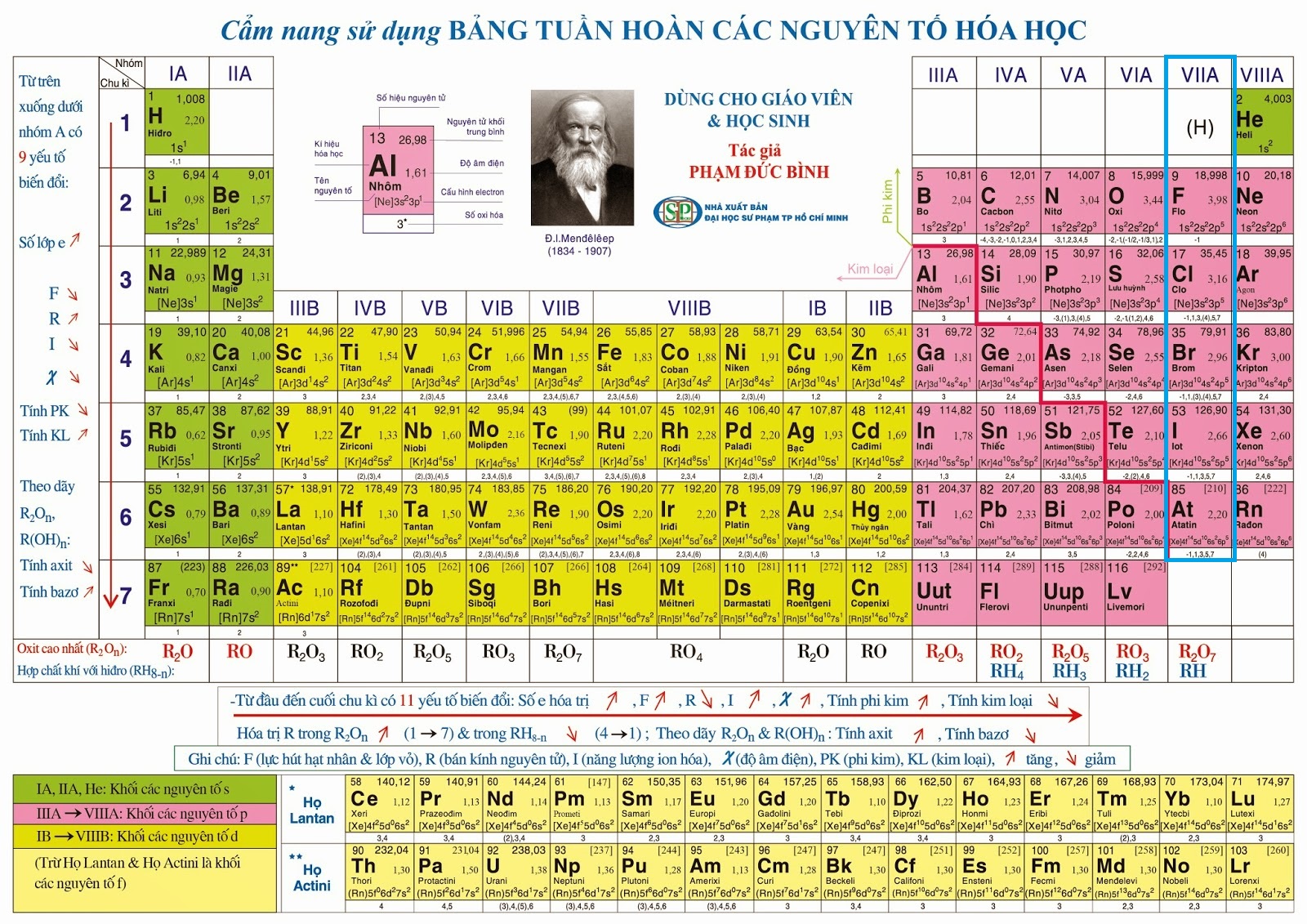
Hình 1: Vị trí của nhóm Halogen trong bảng hệ thống tuần hoàn
1.2. Cấu hình electron nguyên tử, cấu tạo phân tử
- Nguyên tử có 7e lớp ngoài cùng (ns2 np5)
- Ở trạng thái tự do, 2 nguyên tử halogen góp chung 1 e với nhau tạo một liên kết công hóa trị không cực.
công thức electron
- Công thức cấu tạo: X - X
- Công thức phân tử: X2
- Liên kết trong phân tử X2 không bền lắm, dễ bị tách thành 2 nguyên tử X.
- Trong phản ứng hoá học, các nguyên tử X dễ thu thêm 1e ⇒ Tính chất hoá học cơ bản của các halogen là tính oxi hoá mạnh.
1.3. Sự biến đổi tính chất
1.3.1. Sự biến đổi tính chất vật lí của các đơn chất
| Tính chất |
Flo |
Clo |
Brom |
Iot |
|
Số hiệu nguyên tử |
9 | 17 | 35 | 53 |
|
Bán kính nguyên tử (nm) |
0,064 |
0,099 |
0,114 |
0,133 |
| Cấu hình electron lớp ngoài cùng của nguyên tử |
2s22p5 |
3s23p5 |
4s24p5 |
5s25p5 |
| Nguyên tử khối | 19 | 35,5 | 80 | 127 |
| Trạng thái tập hợp của đơn chất ở 200C | Khí | Khí | Lỏng | Rắn |
|
Màu sắc |
Lục nhạc |
Vàng lục |
Nâu đỏ |
Đen tím |
|
Nhiệt độ nóng chảy(0C) |
-219,6 |
-101,0 |
-7,3 |
113,6 |
|
Nhiệt độ sôi |
-188,1 |
-34,1 |
59,2 |
185,5 |
|
Độ âm điện |
3,98 |
3,16 |
2,96 |
2,66 |
Hình 2: Màu sắc của F, Cl, Br, I, At của nhóm halogen
Từ F đến I, ta thấy:
- Trạng thái tập hợp: khí → lỏng → rắn
- Màu sắc: đậm dần
- tonc , tosôi : tăng dần
1.3.2. Sự biến đổi độ âm điện
- Độ âm điện tương đối lớn.
- Giảm dần từ F đến I
-
F trong các hợp chất có số oxi hóa là -1, các nguyên tố còn lại ngoài mức oxi hóa là -1 còn có mức oxi hóa là +1, +3, +5, +7.
⇒ Vì flo có độ âm điện lớn nhất chỉ hút e nên chỉ có số oxi hoá -1, các nguyên tố còn lại có thể tạo thành 1, 3, 5, 7 e độc thân ở trạng thái bị kích thích nên có thể nhường 1, 3, 5, 7 e nên ngoài số oxi hoá -1 còn có thêm số oxi hoá +1, +3, +5, +7
1.3.3. Sự biến đổi tính chất hoá học của các đơn chất
Các đơn chất halogen giống nhau về tính chất hoá học cũng như thành phần và tính chất của các hợp chất do chúng tạo thành (Do lớp e ngoài cùng có cấu hình tương tự nhau ns2 np5)
-
Halogen là những phi kim điển hình, tính oxi hóa giảm từ F → I;
-
Halogen oxi hóa hầu hết các kim loại tạo muối halogenua;
-
Halogen oxi hóa hyđro tạo ra hợp chất khí hyđro halogenua, chất này tan trong nước tạo axit halogenhiđric.
Bài 1:
Vì sao trong các hợp chất, F chỉ có số oxi hoá -1, các nguyên tố halogen còn lại, ngoài số oxi hoá -1 còn có +1, +3, +5, +7.
Hướng dẫn:
Flo có lớp e ngoài cùng là lớp thứ 2 nên không có phân lớp d. Từ Clo → Iot có phân lớp d còn trống, nên được kích thích sẽ có 3e, 5e, 7e độc thân.
Do đó trong các hợp chất Flo luôn có số oxi hoá –1, các halogen khác thể hiện số oxi hoá từ –1 → +7.
3. Luyện tập Bài 21 Hóa học 10
Sau bài học cần nắm:
- Vị trí nhóm halogen trong bảng tuần hoàn;
- Sự biến đổi độ âm điện, bán kính nguyên tử và một số tính chất vật lí của các nguyên tố trong nhóm;
- Cấu hình lớp electron ngoài cùng của nguyên tử các nguyên tố halogen tương tự nhau.
- Tính chất hoá học cơ bản của các nguyên tố halogen là tính oxi hoá mạnh; Sự biến đổi tính chất hóa học của các đơn chất trong nhóm halogen.
3.1. Trắc nghiệm
Bài kiểm tra Trắc nghiệm Hóa học 10 Bài 21 có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
-
- A. Halogen là những phi kim điển hình, chúng là những chất oxi hoá mạnh.
- B. Trong hợp chất, các halogen đều có thể có số oxi hoá:-1,+1,+3,+5,+7.
- C. Khả năng oxi hoá của halogen giãm từ flo đến iot.
- D. Các halogen khá giống nhau về tính chất hoá học.
-
Câu 2:
Halogen là phi kim mạnh vì:
- A. Phân tử có 1 liên kết cộng hoá trị.
- B. Có độ âm điện lớn.
- C. Năng lượng liên kết phân tử không lớn.
- D. Bán kính nguyên tử nhỏ hơn so với các nguyên tố trong cùng chu kì.
-
- A. Nguyên tử chỉ có khả năng thu 1 electron.
- B. Tạo ra hợp chất liên kết cộng hoá trị với hiđro.
- C. Có số oxi hoá -1 trong mọi hợp chất.
- D. Lớp electron ngoài cùng của nguyên tử có 7 electron.
-
- A. Flo
- B. Brom
- C. Clo
- D. Iot
-
- A. 4.
- B. 3.
- C. 5.
- D. 2.
Câu 3- Câu 5: Xem thêm phần trắc nghiệm để làm thử Online
3.2. Bài tập SGK và Nâng cao
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 10 Bài 21.
Bài tập 21.6 trang 51 SBT Hóa học 10
Bài tập 21.7 trang 51 SBT Hóa học 10
Bài tập 21.8 trang 51 SBT Hóa học 10
Bài tập 21.9 trang 51 SBT Hóa học 10
Bài tập 21.10 trang 51 SBT Hóa học 10
Bài tập 21.11 trang 51 SBT Hóa học 10
Bài tập 1 trang 119 SGK Hóa học 10 nâng cao
Bài tập 2 trang 119 SGK Hóa học 10 nâng cao
Bài tập 3 trang 119 SGK Hóa học 10 nâng cao
Bài tập 4 trang 119 SGK Hóa học 10 nâng cao
Bài tập 5 trang 119 SGK Hóa học 10 nâng cao
Bài tập 6 trang 119 SGK Hóa học 10 nâng cao
4. Hỏi đáp về Bài 21 Chương 5 Hóa học 10
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa HOC247 thảo luận và trả lời nhé.
Bạn có biết?
Hóa học, một nhánh của khoa học tự nhiên, là ngành nghiên cứu về thành phần, cấu trúc, tính chất, và sự thay đổi của vật chất.Hóa học nói về các nguyên tố, hợp chất, nguyên tử, phân tử, và các phản ứng hóa học xảy ra giữa những thành phần đó.Hóa học đôi khi được gọi là "khoa học trung tâm" vì nó là cầu nối các ngành khoa học tự nhiên khác như vật lý học, địa chất học và sinh học.
Nguồn : Wikipedia - Bách khoa toàn thưTâm sự Lớp 10
Lớp 10 - Năm thứ nhất ở cấp trung học phổ thông, năm đầu tiên nên có nhiều bạn bè mới đến từ những nơi xa hơn vì ngôi trường mới lại mỗi lúc lại xa nhà mình hơn. Được biết bên ngoài kia là một thế giới mới to và nhiều điều thú vị, một trang mới đang chò đợi chúng ta.
Nguồn : ADMIN :))Copyright © 2021 HOCTAPSGK