Giải Hóa 10 Bài 11: Liên kết cộng hóa trị là tài liệu vô cùng hữu ích, giúp các em học sinh lớp 10 có thêm nhiều gợi ý tham khảo, nhanh chóng trả lời toàn bộ câu hỏi trong sách Cánh diều trang 57→63.
Hóa 10 bài 11: Liên kết cộng hóa trị được biên soạn khoa học, chi tiết giúp các em rèn kỹ năng giải Hóa, so sánh đáp án vô cùng thuận tiện từ đó sẽ học tốt môn Hóa học 10. Đồng thời đây cũng là tài liệu giúp quý thầy cô tham khảo để soạn giáo án. Vậy sau đây là giải Hóa 10 bài 10 trang 57→63 sách Cánh diều, mời các bạn cùng theo dõi tại đây.
Giải Hóa 10 Bài 11: Liên kết cộng hóa trị
Lý thuyết Liên kết cộng hóa trị
1. Sự hình thành phân tử đơn chất
- Liên kết cộng hóa trị là liên kết được hình thành giữa hai nguyên tử bằng một hay nhiều cặp electron chung.
- Mỗi cặp electron chung tạo nên một liên kết cộng hóa trị.
- Các phân tử đơn chất tạo nên từ các nguyên tử của cùng một nguyên tố (có độ âm điện như nhau), nên các cặp electron chung không bị hút lệch về phía nguyên tử nào. Do đó, liên kết trong các phân tử đó không bị phân cực. Đó là liên kết cộng hóa trị không cực.
2. Sự hình thành phân tử hợp chất
- Liên kết cộng hóa trị trong đó cặp electron chung bị lệch về phía nguyên tử có độ âm điện lớn hơn được gọi là liên kết cộng hóa trị có cực hay liên kết cộng hóa trị phân cực.
- Với những phân tử có cấu tạo thẳng như CO2: Liên kết giữa hai nguyên tử oxi và cacbon là phân cực, nhưng phân tử CO2 có cấu tạo thẳng nên độ phân cực của hai liên kết đôi (C=O) triệt tiêu nhau, kết quả là toàn bộ phân tử không bị phân cực.
Giải bài tập Hóa 10 Bài 11 trang 63
Bài 1
Những phát biểu nào sau đây là đúng?
(a) Nếu cặp electron chung bị lệch về phía một nguyên tử khi đó là liên kết cộng hóa trị không cực.
(b) Nếu cặp electron chung bị lệch về phía một nguyên tử thì đó là liên kết cộng hóa trị có cực.
(c) Cặp electron dùng chung luôn được tạo nên từ 2 electron của cùng một nguyên tử.
(d) Cặp electron chung được tạo nên từ 2 electron hóa trị.
Gợi ý đáp án
Phát biểu đúng là: (b), (d)
(a) Sai vì: Nếu cặp electron chung bị lệch về phía một nguyên tử khi đó là liên kết cộng hóa trị có cực.
(b) Đúng.
(c) Sai vì: Cặp electron chung có thể được tạo nên từ 2 electron của cùng một nguyên tử (liên kết cho nhận) hoặc được tạo nên từ 2 electron của hai nguyên tử khác nhau, trong đó mỗi nguyên tử góp chung 1 electron.
(d) Đúng.
Bài 2
Những phát biểu nào sau đây là đúng?
(a) Liên kết đôi được tạo nên từ hai liên kết σ.
(b) Liên kết ba được tạo nên từ 2 liên kết σ và 1 liên kết π.
(c) Liên kết đôi được tạo nên từ 1 liên kết σ và 1 liên kết π.
(d) Liên kết ba được tạo nên từ 1 liên kết σ và 2 liên kết π.
Gợi ý đáp án
Phát biểu đúng: (c), (d)
Liên kết đôi được tạo nên từ 1 liên kết σ và 1 liên kết π.
Liên kết ba được tạo nên từ 1 liên kết σ và 2 liên kết π.
Bài 3
Viết công thức Lewis cho các phân tử H2O và CH4 . Mỗi phân tử này có bao nhiêu cặp electron hóa trị riêng?
Gợi ý đáp án
Công thức Lewis của H2O:
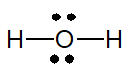
Phân tử H2O có 2 cặp electron hóa trị riêng.
Công thức Lewis của CH4
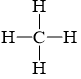
Phân tử CH4 không có cặp electron hóa trị riêng.
Bài 4
Sử dụng bảng giá trị năng lượng liên kết ở phụ lục 2.
a) Hãy tính tổng năng lượng liên kết trong mỗi phân tử H2S và H2
b) Nhiệt độ để bắt đầu phá vỡ liên kết (nhiệt độ phân hủy) trong hai chất trên ứng với một trong hai nhiệt độ sau: 400oC hoặc 1 000o Em hãy dự đoán nhiệt độ phân hủy của chất nào cao hơn. Vì sao?
Gợi ý đáp án
a)
Công thức phân tử của H2S là H-S-H
⇒ Phân tử H2S gồm hai liên kết S-H.
Tổng năng lượng liên kết trong phân tử H2S là: 2.368 = 736 kJ mol-1
Công thức phân tử của H2O là H-O-H
⇒ Phân tử H2O gồm hai liên kết O-H
Tổng năng lượng liên kết trong phân tử H2O là: 2.464 = 928 kJ mol-1
b) Năng lượng liên kết trong phân tử H2O lớn hơn H2S (928 kJ mol-1 > 736 kJ mol-1)
⇒ Nhiệt độ để bắt đầu phá vỡ liên kết (nhiệt độ phân hủy) H2O lớn hơn H2S
⇒ Nhiệt độ phân hủy của H2O là 1000oC, của H2S là 400oC
Bài 5
Khi phản ứng với H2, các phân tử như F2, N2cần phải phá vỡ liên kết giữa các nguyên tử. Dựa vào năng lượng liên kết, em hãy dự đoán phản ứng của F2hay của N2 với H2 sẽ thuận lợi hơn (dễ xảy ra hơn)?
Gợi ý đáp án
Năng lượng liên kết F-F là 159 kJ mol-1
Năng lượng liên kết N≡N là 946 kJ mol-1
⇒ Năng lượng cần để phá vỡ liên kết N≡N lớn hơn năng lượng cần để phá vỡ liên kết
F-F
⇒ Phản ứng của F2với H2 sẽ thuận lợi hơn.
