Giải Hóa 10 Bài 4: Ôn tập chương 1 là tài liệu vô cùng hữu ích, giúp các em học sinh lớp 10 có thêm nhiều gợi ý tham khảo, nhanh chóng trả lời toàn bộ câu hỏi trong sách Kết nối tri thức với cuộc sống trang 26, 27 thuộc Chương 1.
Hóa 10 bài 4: Ôn tập chương 1 được biên soạn khoa học, chi tiết giúp các em rèn kỹ năng giải Hóa, so sánh đáp án vô cùng thuận tiện từ đó sẽ học tốt môn Hóa học 10. Đồng thời đây cũng là tài liệu giúp quý thầy cô tham khảo để soạn giáo án. Vậy sau đây là giải Hóa 10 trang 27 sách Kết nối tri thức, mời các bạn cùng theo dõi tại đây.
Giải 10 Bài 4: Ôn tập chương 1 sách Kết nối tri thức
Giải Hóa học 10 Bài 4 trang 27
Câu 1
Số proton, neutron và electron của ![]() lần lượt là
lần lượt là
| A. 19, 20, 39 | B. 20, 19, 39 | C. 19, 20, 19 | D. 19, 19, 20 |
Gợi ý đáp án
Nguyên tử ![]() cho biết:
cho biết:
Số hiệu nguyên tử = số proton = số electron = 19
Số khối = 39 => Số neutron = 39 – 19 = 20
=> Số proton, neutron và electron của ![]() lần lượt là 19, 20, 19
lần lượt là 19, 20, 19
Câu 2
Nguyên tử của nguyên tố nào sau đây có 3 electron thuộc lớp ngoài cùng
![]()
![]()
![]()
![]()
Gợi ý đáp án
Đáp án C
![]() có Z = 11
có Z = 11
Cấu hình electron: 1s22s22p63s1
=> Có 1 electron ở lớp ngoài cùng
![]() có Z = 7
có Z = 7
Cấu hình electron: 1s22s22p3
=> Có 5 electron ở lớp ngoài cùng
![]() có Z = 13
có Z = 13
Cấu hình electron: 1s22s22p63s23p1
=> Có 3 electron ở lớp ngoài cùng
![]() có Z = 6
có Z = 6
Cấu hình electron: 1s22s22p2
=> Có 4 electron ở lớp ngoài cùn
Câu 3
Nguyên tử của nguyên tố potassium có 19 electron. Ở trạng thái cơ bản, potassium có số orbital chứa electron là
| A. 8 | B. 9 | C. 11 | D. 10 |
Gợi ý đáp án
Nguyên tử potassium có 19 electron
=> Cấu hình electron: 1s22s22p63s23p64s1
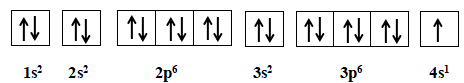
Potassium có 10 orbital chứa electron.
Đáp án D
Câu 4
Nguyên tử của nguyên tố sodium (natri) (Z = 11) có cấu hình electron là
| A. 1s22s22p63s2 | B. 1s22s22p6 | C. 1s22s22p63s1 | D. 1s22s22p53s2 |
Gợi ý đáp án
Cấu hình electron: 1s22s22p63s1
Đáp án C
Câu 5
Tổng số hạt proton, neutron và electron trong nguyên tử X là 58. Số hạt mang điện nhiều hơn số hạt không mang điện là 18. X là
| A. Cl | B. Ca | C. K | D. S |
Gợi ý đáp án
Gọi số hạt proton, electron và neutron trong nguyên tử X lần lượt là p, e, n
Ta có:
Nguyên tử X có tổng số hạt proton, neutron và electron là 58:
=> p + e + n = 58 <=> 2p +n = 58 (vì p = e) (1)
Số hạt mang điện nhiều hơn số hạt không mang điện là 18:
=> p + e – n = 18 <=> 2p - n = 18 (2)
Giải phương trình (1), (2)
p = e = 19 và n = 20
=> X là Kali
Đáp án C
Câu 6
Nguyên tố chlorine có Z = 17. Hãy cho biết số lớp electron, số electron thuộc lớp ngoài cùng, số electron độc thân của nguyên tử chlorine
Gợi ý đáp án
Nguyên tố chlorine có Z = 17
Cấu hình electron: 1s22s22p63s23p5
Cấu hình chlorine theo ô orbital
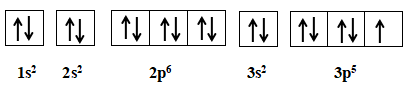
+ Số lớp electron của Chlorine: 3
+ Số electron của Chlorine thuộc lớp ngoài cùng: 7
+ Số electron của Chlorine độc thân: 1
Câu 7
Nguyên tử khối trung bình của vanadium (V) là 50.9975. Nguyên tố V có 2 đồng vị trong đó đồng vị ![]() chiếm 0.25%. Tính số khối của đồng vị còn lại
chiếm 0.25%. Tính số khối của đồng vị còn lại
Gợi ý đáp án
Gọi số khối đồng vị còn lại là a. Ta có:
![]() => a = 51
=> a = 51
Vậy số khối đồng vị còn lại củaVanadi là 51
Câu 8
Cấu hình electron của:
- Nguyên tử X: 1s22s22p63s23p64s1
- Nguyên tử Y: 1s22s22p63s23p4
a) Mỗi nguyên tử X và Y chứa bao nhiêu electron?
b) Hãy cho biết số hiệu nguyên tử của X và Y.
c) Lớp electron nào trong nguyên tử X và Y có mức năng lượng cao nhất?
d) Mỗi nguyên tử X và Y có bao nhiêu lớp electron, bao nhiêu phân lớp electron?
e) X và Y là nguyên tố kim loại, phi kim hay khí hiếm?
Gợi ý đáp án
a)
Nguyên tử X có 19 electron
Nguyên tử X có 16 electron
b)
Nguyên tử X có 19 electron => Nguyên tử X có số hiệu nguyên tử ZX = 19
Nguyên tử Y có 16 electron => Nguyên tử Y có số hiệu nguyên tử ZY = 16
c)
Trong nguyên tử X lớp electron ở mức năng lượng cao nhất là lớp N (n= 4)
Trong nguyên tử Y lớp electron ở mức năng lượng cao nhất là lớp M (n= 3)
d) Nguyên tử X có:
+ 4 lớp electron (n = 1, 2, 3, 4)
+ 6 phân lớp electron (gồm 1s, 2s, 2p, 3s, 3p, 4s)
Nguyên tử Y có:
+ 3 lớp electron (n= 1, 2, 3)
+ 5 phân lớp electron (gồm 1s, 2s, 2p, 3s, 3p)
e)
Nguyên tử X có 1 e lớp ngoài cùng (4s1)
=> X là nguyên tố kim loại.
Nguyên tử Y có 6 e lớp ngoài cùng (3s23p4)
=> Y là nguyên tố phi kim.
Câu 9
Nguyên tố X được dùng để chế tạo hợp kim nhẹ, bền, dùng trong nhiều lĩnh vực: hàng không, ô tô, xây dựng, hàng tiêu dùng,… Nguyên tố Y ở dạng YO43-, đóng vai trò quan trọng trong các phân tử sinh học như DNA và RNA. Các tế bào sống sử dụng YO43- để vận chuyển năng lượng. Nguyên tử của nguyên tố X có cấu hình electron kết thúc ở phân lớp 3p1. Nguyên tử nguyên tố Y có cấu hình electron kết thúc ở phân lớp 3p3. Viết cấu hình electron nguyên tử của X và Y. Tính số electron trong các nguyên tử X và Y. Nguyên tố X và Y có tính kim loại hay phi kim?
Gợi ý đáp án
Nguyên tử nguyên tố X có electron cuối cùng điền vào phân lớp 3p1
Cấu hình electron của X là: 1s22s22p63s23p1
=> X có 13 e và X là nguyên tố kim loại (vì có 3 e lớp ngoài cùng)
Nguyên tử nguyên tố Y có e cuối cùng điền vào phân lớp 3p3
Cấu hình electron của Y là: 1s22s22p63s23p3
=> Y có 15 e và Y là nguyên tố phi kim (vì có 5 e lớp ngoài cùng).
Câu 10
Nguyên tử của nguyên tố X có tổng số hạt cơ bản (proton, electron, neutron) là 49, trong đó số hạt không mang điện bằng 53,125% số hạt mang điện. Xác định điện tích hạt nhận, số proton, số electron, số neutron và số khối của X?
Gợi ý đáp án
Gọi số hạt proton, electron và neutron trong nguyên tử X lần lượt là P, E, N (Z = P = E)
Ta có theo đầu bài:
Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 49:
=> 2Z + N = 49 (1)
Lại có, số hạt không mang điện bằng 53,125% số hạt mang điện:
=> N = 2Z .53,125/100 (2)
Giải phương trình (1) và (2) ta được:
=> Z = 16 = P = E
N =17
Số khối của nguyên tử X là: Z + N = 16 + 17 = 33
Vậy nguyên tử nguyên tố X có: điện tích hạt nhân là 16+, 16 proton, 16 electron, 17 neutron và có số khối là 33.
