2. Cho luồng khí hydrogen đi qua ống thủy tinh chứa 40(g) bột Copper (II) oxide ở 4000 Sau phản ứng thu được 33,6(g) chất rắn. Nêu hiện tượng phản ứng xảy ra.
- 2. Cho luồng khí hydrogen đi qua ống thủy tinh chứa 40(g) bột Copper (II) oxide ở 4000 Sau phản ứng thu được 33,6(g) chất rắn.
- Nêu hiện tượng phản ứng xảy ra.
- Tính hiệu suất phản ứng.
- Tính số phân tử khí hydrogen đã tham gia khử Copper (II) oxide ở trên.
Lời giải 1 :
Đáp án + Giải thích các bước giải:
`a)` PTHH: CuO + H2 ---------> Cu + H2O
Ta có nCuO `= (40)/(80) = 0,5` (mol)
Nếu CuO phản ứng hết ⇒ nCuO = nCu = 0,5 mol
⇒ mCu = `0,5 . 64 = 32 < 33,6`
⇒ CuO dư (không phản ứng hết)
Gọi x là số mol CuO phản ứng
Theo đề bài có nCuO = nCu = x
⇒ `(0,5 - x) . 80 + 64x = 33,6`
⇒ `x = 0,4` (mol)
Hiệu suất phản ứng là: `H%` `= (0,4)/(0,5) . 100% = 80%`
`b)` Theo PTHH có:
nH2 = nCuO phản ứng = 0,4 (mol)
⇒ vH2 = `0,4 . 22,4 = 8,96` (L)
`#seungho`
Lời giải 2 :
Gửi
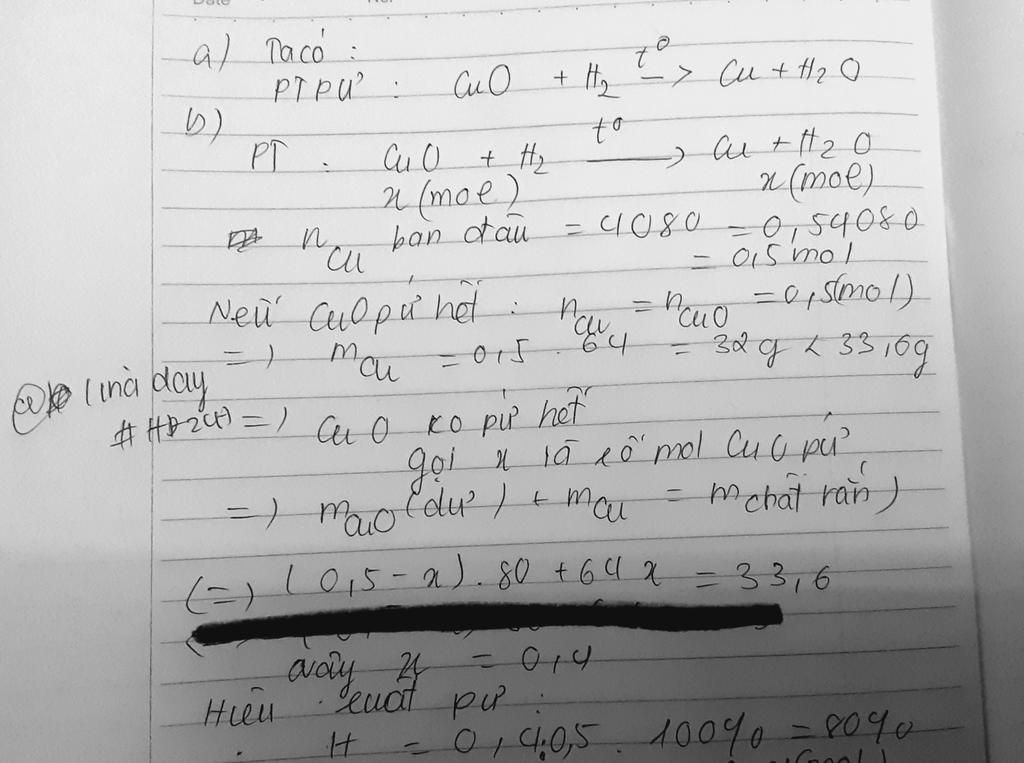

Bạn có biết?
Hóa học là ngành nghiên cứu về thành phần, cấu trúc, tính chất, và sự thay đổi của vật chất. Hóa học nói về các nguyên tố, hợp chất, nguyên tử, phân tử, và các phản ứng hóa học xảy ra giữa những thành phần đó. Hóa học đôi khi được gọi là "khoa học trung tâm" vì nó là cầu nối các ngành khoa học tự nhiên khác như vật lý học, địa chất học và sinh học. Hãy đam mê và khám phá thế giới của các chất hóa học và phản ứng!
Nguồn :
Wikipedia - Bách khoa toàn thưTâm sự lớp 8
Lớp 8 - Năm thứ ba ở cấp trung học cơ sở, học tập bắt đầu nặng dần và sang năm lại là năm cuối cấp, áp lực lớn dần. Hãy chú ý đến sức khỏe, cân bằng giữa học và nghỉ ngơi để đạt hiệu quả tốt nhất!
Nguồn :
sưu tậpCó thể bạn quan tâm
Hóa Học
Lớp 8
Câu 4: (4,0 điểm) Khử hoàn toàn 3,48 gam oxide MxOy cần dùng 1,4874 lít khí H2 (đkc) thu được kim loại M. Hòa tan M thu được ở trên vào dung dịch Hydro Chloric ...Hóa Học
Lớp 8
Nung hoàn toàn 15,15 gam chất rắn A thu được chất rắn B và 1,85925 lít khí oxygen (ở đkc). Trong hợp chất B có thành phần % khối lượng các nguyên tố: 37,65% o ...Copyright © 2021 HOCTAPSGK
